题目内容
7.(1)二甲醚[CH3OCH3]燃料电池的工作原理如下图一所示.
①该电池负极的电极反应式为CH3OCH3+3H2O-12e-═2CO2+12H+
②该电池正极的电极反应式为O2+4e-+4H+=2H2O
(2)以上述电池为电源,通过导线与图二电解池相连.
①若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑
②若X、Y分别为铜、银,a为1L 0.2mol/L AgNO3溶液,写出Y电极反应式Ag-e-=Ag+
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图三(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).
①结合图三计算,上述电解过程中消耗二甲醚的质量为0.77g.
②若图三的B点pH=7,则滴定终点在AB区间(填“AB”、“BC”或“CD”).
分析 (1)根据氢离子移动方向知,左边电极是负极,通入燃料二甲醚,右边电极是正极,通入氧化剂氧气,该燃料电池中,正极上氧气得电子和氢离子反应生成水;
电池在放电过程中,负极上二甲醚失电子生成氢离子;
(2)①X、Y为石墨,放电时,阳极上氢氧根离子放电、阴极上氢离子放电;
②X、Y分别为铜、银,Y是阳极,阳极上银失电子发生氧化反应;
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后溶液,滴加0.4mol/L醋酸得到图三,
①根据图知,KOH溶液的pH=13,常温下,KOH的浓度是0.1mol/L,则n(KOH)=0.1mol/L×2L=0.2mol,根据KOH和转移电子正极的关系式计算转移电子,再根据转移电子守恒计算二甲醚的质量;
②滴定终点二者恰好反应生成CH3COOK.
解答 解:(1)①根据氢离子移动方向知,左边电极是负极,通入燃料二甲醚,右边电极是正极,通入氧化剂氧气,该燃料电池中,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4e-+4H+=2H2O;故答案为:O2+4e-+4H+=2H2O;
②电池在放电过程中,b对应的电极上二甲醚失电子生成氢离子,即CH3OCH3+3H2O-12e-═2CO2+12H+;
故答案为:CH3OCH3+3H2O-12e-═2CO2+12H+;
(2)①X、Y为石墨,放电时,阳极上氢氧根离子放电、阴极上氢离子放电,所以电池反应式为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
②X、Y分别为铜、银,Y是阳极,阳极上银失电子发生氧化反应,电极反应式为Ag-e-=Ag+,
故答案为:Ag-e-=Ag+;
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后溶液,滴加0.4mol/L醋酸得到图三,①根据图知,KOH溶液的pH=13,常温下,KOH的浓度是0.1mol/L,则n(KOH)=0.1mol/L×2L=0.2mol,根据2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑知,生成0.2mol氢氧根离子转移电子的物质的量0.2mol,二甲醚燃料电池的总反应方程式是CH3OCH3+3O2=2CO2+3H2O,二甲醚转化为CO2,消耗1mol二甲醚转移电子数=2×[4-(-2)]=12mol,因此当转移0.2mol电子时消耗二甲醚的质量=$\frac{0.2mol}{12}$×46g/mol=0.77g,
故答案为:0.77;
②滴定终点二者恰好反应生成CH3COOK,KOH的浓度是醋酸的一半,则恰好中和时需要酸的体积等于KOH体积的一半,醋酸钾为强碱弱酸盐,其溶液呈碱性,当溶液的pH=7时,醋酸稍微过量,所以醋酸体积大于KOH体积的一半,所以滴定终点为AB段,故答案为:AB.
点评 本题考查了原电池和电解池原理等知识点,这些知识点都是考试热点,知道原电池和电解池中各个电极上发生的电极反应式,近几年中化学电源新型电池及燃料电池考查较多要熟练掌握基本知识,灵活运用基础知识解答问题,题目难度中等.

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案| A. | 碳酸钙分解 | B. | 盐酸和氢氧化钠溶液混合 | ||
| C. | 锌放入稀硫酸中 | D. | 氯化铵晶体与氢氧化钡晶体混合 |
| A. | 乙烯和乙炔 | B. | 苯和己烷 | C. | 苯和甲苯 | D. | 溴苯和溴乙烷 |
| A. | 冰的密度比液态水的密度小是因为冰分子之间含有较强的化学键 | |
| B. | 氨分子的键角比甲烷分子的键角小是因为两个分子中中心原子的杂化方式不同 | |
| C. | HF的沸点比HCl的沸点高是因为HF分子内含有氢键 | |
| D. | HF比HCl稳定是因为HF分子中共价键的键能大 |
| A. | A、B两种元素可组成化学式为BA2的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是E>F | |
| D. | 气态氢化物的稳定性由强到弱的顺序是C>D |
| A. | NH4+、Ba2+、NO3-、CO32- | B. | Fe2+、Na+、SO42-、MnO4- | ||
| C. | K+、Mg2+、NO3-、SO42- | D. | Na+、Fe3+、Cl-、AlO2- |
| A. | 蒸发操作时,当混合物中的晶体大部分析出时,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体也从下口放出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
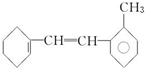 有机物结构简式如下:
有机物结构简式如下: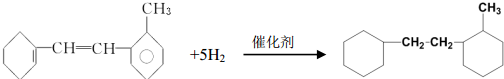 .
.