题目内容
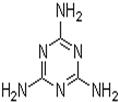 近期有两件事引起了人们的极大关注.“问题奶粉”其问题主要是掺杂了三聚氰胺,该物质的结构如图,
近期有两件事引起了人们的极大关注.“问题奶粉”其问题主要是掺杂了三聚氰胺,该物质的结构如图,①该物质的含氮量为
②该物质遇强酸或强碱水溶液水解,氨基逐步被羟基取代,先生成三聚氰酸二酰胺,进一步水解生成三聚氰酸一酰胺,当氨基全部被羟基取代完后则生成三聚氰酸.经研究表明三聚氰胺和三聚氰酸在肾细胞中结合沉积从而形成肾结石,堵塞肾小管,最终造成肾衰竭.试写出三聚氰胺生成三聚氰酸的化学方程式
考点:化学方程式的书写,元素质量分数的计算
专题:
分析:①根据三聚氰胺的结构图可知化学式为C3N6H6,尿素的化学式为CO(NH2)2,利用相对原子质量来计算质量分数;由工业合成三聚氰胺主要使用尿素为原料,在加热和一定压力条件下生成该物质及氨和二氧化碳,以此书写化学反应方程式;
②根据该物质遇强酸或强碱水溶液水解,氨基逐步被羟基取代,先生成三聚氰酸二酰胺,进一步水解生成三聚氰酸一酰胺,最后生成三聚氰酸来分析.
②根据该物质遇强酸或强碱水溶液水解,氨基逐步被羟基取代,先生成三聚氰酸二酰胺,进一步水解生成三聚氰酸一酰胺,最后生成三聚氰酸来分析.
解答:
解:①由三聚氰胺的结构图可知化学式为C3N6H6,则N元素的质量分数为
×100%=66.7%,
尿素的化学式为CO(NH2)2,理论上含氮量为
×100%=46.7%,
由尿素在加热和一定压力条件下生成该物质及氨和二氧化碳,结合质量守恒定律可知发生的化学反应为6(NH2)2CO═C3H6N6+6NH3↑+3CO2↑,
故答案为:66.7%;46.7%;6(NH2)2CO═C3H6N6+6NH3↑+3CO2↑;
②由题意可知,C3H6N6水解可生成三聚氰酸一酰胺,最后生成三聚氰酸,水解反应为C3H6N6+3H2O=C3N3(OH)3+3NH3,
故答案为:C3H6N6+3H2O=C3N3(OH)3+3NH3.
| 14×6 |
| 12×3+14×6+1×6 |
尿素的化学式为CO(NH2)2,理论上含氮量为
| 14×2 |
| 12+16+16×2 |
由尿素在加热和一定压力条件下生成该物质及氨和二氧化碳,结合质量守恒定律可知发生的化学反应为6(NH2)2CO═C3H6N6+6NH3↑+3CO2↑,
故答案为:66.7%;46.7%;6(NH2)2CO═C3H6N6+6NH3↑+3CO2↑;
②由题意可知,C3H6N6水解可生成三聚氰酸一酰胺,最后生成三聚氰酸,水解反应为C3H6N6+3H2O=C3N3(OH)3+3NH3,
故答案为:C3H6N6+3H2O=C3N3(OH)3+3NH3.
点评:本题以信息的形式来考查学生化学反应方程式及有关计算,把握物质的组成、信息的分析与应用是解答本题的关键,注重学生分析解决问题的能力的考查,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
下列A.B.C对应的三种(类)物质满足如图所示关系的是( )


| A、A--烷烃、B--脂肪烃、C--烃 |
| B、A--苯、B--酚、C--芳香化合物 |
| C、A--烷烃、B--卤代烃、C--有机物 |
| D、A--烯烃、B--炔烃、C--烃 |
某氢氧化钠溶液跟醋酸溶液混合后,溶液pH<7.混合溶液中离子物质的量浓度关系正确的是( )
| A、c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D、c(Na+)+c(H+)>c(OH-)+c(CH3COO-) |
下列离子方程式中,正确的是( )
| A、氯化铝溶液中加入过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、将铜屑加入Fe3+溶液中:2Fe3++Cu═2Fe2++Cu2+ |
| C、向硫酸氢钠溶液中滴入氢氧化钡溶液至中性H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3 |
下列试剂:①氯水;②硝酸银;③浓硝酸;④浓H2SO4;⑤氢氟酸;⑥苯酚,需要保存在棕色试剂瓶中的是( )
| A、①②③ | B、②③⑤ |
| C、③④⑥ | D、④⑤⑥ |
下列关于碳酸钠和碳酸氢钠的性质叙述中,正确的是( )
| A、在水中的溶解性:碳酸钠小于碳酸氢钠 |
| B、热稳定性:碳酸钠大于碳酸氢钠 |
| C、与酸反应的速率:碳酸钠大于碳酸氢钠 |
| D、碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |
在下列各组物质中,所含分子数和原子数均相同的是( )
| A、1mol二氧化碳和1mol氯化氢 |
| B、1g氢气和16g氧气 |
| C、1mol一氧化碳和44g二氧化碳 |
| D、18g水和28g一氧化碳 |