题目内容
在下列各组物质中,所含分子数和原子数均相同的是( )
| A、1mol二氧化碳和1mol氯化氢 |
| B、1g氢气和16g氧气 |
| C、1mol一氧化碳和44g二氧化碳 |
| D、18g水和28g一氧化碳 |
考点:物质的量的相关计算
专题:
分析:A.根据N=nNA可知,物质的量相等,含有分子数目相等,但二氧化碳为三原子分子,HCl为双原子分子;
B.根据n=
计算氢气、氧气物质的量,二者均为双原子分子,若二者物质的量相等,则含有分子数数目相等,含有原子数目相等;
C.根据n=
计算二氧化碳的物质的量,结合分子判断原子数目;
D.根据n=
计算水、CO物质的量,若二者物质的量相等,则含有分子数数目相等,结合分子式判断原子数目.
B.根据n=
| m |
| M |
C.根据n=
| m |
| M |
D.根据n=
| m |
| M |
解答:
解:A.二者物质的量相等,根据N=nNA可知,二者含有分子数目相等,二氧化碳分子含有3个原子,氯化氢含有两个原子,二者含有原子数目不相等,故A错误;
B.1g氢气的物质的量为0.5mol,16g氧气的物质的量为0.5mol,二者都含有1mol原子,故B正确;
C.44g二氧化碳为1mol,二者分子数目相等,但CO分子含有2个原子,二氧化碳分子含有3个原子,含有原子数目不相等,故C错误;
D.18水为1mol,28gCO为1mol,二者分子数目相等,但水分子含有3个原子,CO分子含有2个原子,含有原子数目不相等,故D错误;
故选B.
B.1g氢气的物质的量为0.5mol,16g氧气的物质的量为0.5mol,二者都含有1mol原子,故B正确;
C.44g二氧化碳为1mol,二者分子数目相等,但CO分子含有2个原子,二氧化碳分子含有3个原子,含有原子数目不相等,故C错误;
D.18水为1mol,28gCO为1mol,二者分子数目相等,但水分子含有3个原子,CO分子含有2个原子,含有原子数目不相等,故D错误;
故选B.
点评:本题考查物质的量有关计算、微粒数目计算,比较基础,注意理解化学式意义.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组离子因为生成难溶物而不能大量共存的是( )
| A、Cl-、Fe2+、NO3-、H+ |
| B、HCO3-、Cl-、Na+、H+ |
| C、Ba2+、Cl-、CO32-、K+ |
| D、NH4+、K+、OH-、Cl- |
目前我国城市大气主要污染物是( )
| A、CO2、Cl2、N2、酸雨 |
| B、NH3、CO2、NO、雾 |
| C、HCl、SO2、N2、粉尘 |
| D、SO2、NO2、CO、烟尘 |
下列物质加入水中,使水温显著降低的是( )
| A、固体氢氧化钠 | B、生石灰 |
| C、无水乙醇 | D、固体硝酸铵 |
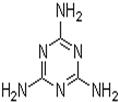 近期有两件事引起了人们的极大关注.“问题奶粉”其问题主要是掺杂了三聚氰胺,该物质的结构如图,
近期有两件事引起了人们的极大关注.“问题奶粉”其问题主要是掺杂了三聚氰胺,该物质的结构如图,