题目内容
5.用下面的原子或离子结构示意图的编号(A、B、C、D)填空:
(1)电子层排布相同的是BC;
(2)属于同种元素的是AB;
(3)属于金属元素的是D;其离子的结构示意图
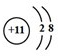 .
.(4)属于稀有气体元素的是C,稀有气体一般不参加化学反应的原因是最外层为稳定结构.
分析 (1)在结构示意图中,圆圈代表原子核,弧线代表电子层,弧线上的数字代表该层上的电子数,只要电子层数相同,对应层数上的电子数相同即是电子层排布相同;
(2)元素是具有相同核电荷数(即核内质子数)的一类原子的总称,故可知同种元素的原子具有相同的质子数;
(3)金属元素原子最外层电子数小于4;D在化学反应中容易失去1个电子,形成8电子稳定结构;
(4)稀有气体元素的原子结构示意图的特点是最外层电子数是8个(氦为2个).
解答 解:(1)从题目给的结构示意图中,可直观的看出电子层排布相同的粒子为B和C,
故答案为:BC;
(2)由元素的定义可知,同种元素的粒子具有相同的核电荷数即核内质子数,所以属于同种元素的是A和B,故答案为:AB;
(3)金属元素原子最外层电子数小于4,属于金属元素的是D;D在化学反应中容易失去1个电子,形成8电子稳定结构,故D失去1个电子形成的离子的结构示意图为 ,故答案为:D;
,故答案为:D; ;
;
(4)C为氖,是稀有气体元素,稀有气体元素最外层8个(氦为2个),为稳定结构,故答案为:C;最外层为稳定结构.
点评 本题考查元素的概念、金属元素的判断和离子结构示意图,难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
3.仪器在使用时,其下端管口要紧靠承接容器内壁的是( )
| A. | 热水漏斗 | B. | 布氏漏斗 | C. | 分液漏斗 | D. | 滴定管 |
16.对一定量气体体积的研究.已知1mol气体在不同条件下的体积和质量:
(1)从上表分析得出结论:
①1mol任何气体,在标准状况下的体积都约为22.4L.
②1mol不同气体,在不同条件下,体积不一定(填“不一定”、“一定不”或“一定”)相同.
(2)理论依据:在相同条件下,决定1mol气体体积大小的主要因素是分子间距相同.
(3)一个NH3分子的质量$\frac{17}{{N}_{A}}$g(不必计算出结果).
| 化学式(气体) | 条件 | 1mol气体体积(L) | 1mol气体质量(g) |
| SO2 | 0℃,101KPa | 22.4 | 64 |
| N2 | 22.4 | 28 | |
| CO2 | 22.4 | 44 | |
| NH3 | 0℃,202KPa | 11.2 | 17 |
| HCl | 11.2 | 36.5 | |
| H2 | 273℃,202KPa | 22.4 | 2 |
| CH4 | 22.4 | 28 |
①1mol任何气体,在标准状况下的体积都约为22.4L.
②1mol不同气体,在不同条件下,体积不一定(填“不一定”、“一定不”或“一定”)相同.
(2)理论依据:在相同条件下,决定1mol气体体积大小的主要因素是分子间距相同.
(3)一个NH3分子的质量$\frac{17}{{N}_{A}}$g(不必计算出结果).
13.下列离子方程式正确的是( )
| A. | 等物质的量的Ba(OH)2和Ba ( HCO3)2 溶于足量水中发生反应:Ba2++2HCO${\;}_{3}^{-}$+2OH-═BaCO3↓+2H2O+CO${\;}_{3}^{2-}$ | |
| B. | NaOH 溶液中滴加少量的Ca(HCO3)2溶液:OH-+Ca2++HCO${\;}_{3}^{-}$═CaCO3↓+H2O | |
| C. | 稀氨水溶液与醋酸的反应:NH3•H2O+CH3COOH═CH3COO-+NH${\;}_{4}^{+}$+H2O | |
| D. | 大理石中滴入硫酸:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O |
17.下列有机物的命名中,正确的是( )
| A. | 3-甲基-1-丁烯 | B. | 2-乙基丁烷 | ||
| C. | 1,2,3-三甲基丁烷 | D. | 3,4-二甲基丁烷 |
15.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1mol浓硫酸和足量铜粉反应转移的电子数为NA | |
| B. | 标准状况下,5.6LNO和5.6 LO2混合后的分子总数为为0.5NA | |
| C. | 0.1mol苯乙烯中含有的碳碳双键的数目为0.1 NA | |
| D. | 将NA个NH3分子溶于1L水中得到1 mol•L-1的氨水 |