题目内容
纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体.下列区分这种两种物质的方法正确的是( )
| A、用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打 |
| B、用两只玻璃杯分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是小苏打 |
| C、分别用炒锅加热两种样品,全部分解挥发,没有残留物质的是小苏打 |
| D、先将两样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打 |
考点:钠的重要化合物
专题:几种重要的金属及其化合物
分析:NaHCO3与Na2CO3相比,NaHCO3的热稳定性差,且与碱反应生成碳酸盐,二者都含钠元素,焰色反应都成黄色,与酸反应,碳酸氢钠更剧烈.
解答:
解:A.二者都含钠元素,焰色反应都成黄色,不能鉴别,故A错误;
B.加入醋酸,碳酸氢钠反应剧烈,所以产生气泡快的是小苏打,可鉴别,故B正确.
C.碳酸氢钠解热分解生成碳酸钠,二者加热时都有残留物,不能鉴别,故C错误;
D.加入澄清石灰水,分别发生:Na2CO3和Ca(OH)2混合后生成CaCO3,发生Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,NaHCO3可与澄清石灰水发生Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O或Ca(OH)2+2NaHCO3═CaCO3↓+Na2CO3+2H2O,不能鉴别,故D错误;
故选B.
B.加入醋酸,碳酸氢钠反应剧烈,所以产生气泡快的是小苏打,可鉴别,故B正确.
C.碳酸氢钠解热分解生成碳酸钠,二者加热时都有残留物,不能鉴别,故C错误;
D.加入澄清石灰水,分别发生:Na2CO3和Ca(OH)2混合后生成CaCO3,发生Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,NaHCO3可与澄清石灰水发生Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O或Ca(OH)2+2NaHCO3═CaCO3↓+Na2CO3+2H2O,不能鉴别,故D错误;
故选B.
点评:本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,题目难度不大,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累.

练习册系列答案
相关题目
有关苏打和小苏打的叙述正确的是( )
| A、等质量的苏打、小苏打分别与足量稀硫酸反应,小苏打产生的二氧化碳多 |
| B、与足量稀硫酸反应,生成等量的二氧化碳消耗的苏打的物质的量比小苏打多 |
| C、向小苏打溶液中滴入氢氧化钡溶液无沉淀,而苏打溶液中滴入氢氧化钡溶液出现沉淀 |
| D、苏打和小苏打都既能与酸反应又能与氢氧化钠反应 |
下列离子方程式正确的是( )
| A、实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | ||||
| B、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | ||||
| C、氯化铝溶液加入氨水:Al3++3OH-═Al(OH)3↓ | ||||
D、用氢氧化钠检验氯化铵溶液中铵根离子:NH4++OH-
|
下列离子在溶液中能大量共存的是( )
| A、HCO3-、NH4+、H+、Cl- |
| B、AlO2-、OH-、Na+、Cl- |
| C、AlO2-、H+、MnO42-、NO3- |
| D、Mg2+、Fe3+、NO3-、SCN- |
对室温下100mL pH=2的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )


| A、加水稀释至溶液体积为200mL,醋酸溶液的pH变为4 |
| B、温度都升高20°C后,两溶液的pH不再相等 |
| C、加水稀释至溶液体积为200mL后,两种溶液中c(OH-)都减小 |
| D、加足量的锌充分反应后,两溶液中产生的氢气体积可用上图表示 |
化学美无处不在,如图是物质间发生化学反应的颜色变化,其中X是( )

| A、稀盐酸 |
| B、Na2SO4溶液 |
| C、稀硫酸 |
| D、Na2CO3溶液 |
下列有关化学用语表示正确的是( )
| A、葡萄糖的结构简式:C6H12O6 | ||
| B、NaHCO3的电离:NaHCO3=Na++H++CO32- | ||
C、质子数为53、中子数为78的碘原子:
| ||
D、CO2的电子式: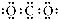 |

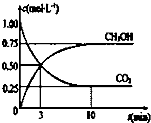 目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kj?mol-1,现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3PH(g)的浓度随时间的变化如图所示.
目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kj?mol-1,现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3PH(g)的浓度随时间的变化如图所示.