题目内容
14.原子数、价电子总数相同的微粒互称等电子体,等电子体具有相同的结构特征.已知硝酰阳离子NO2+与XO2分子互为相同结构的等电子体,则元素X可能为( )| A. | Cl | B. | Si | C. | C | D. | S |
分析 原子总数相同、价电子总数相同的微粒互为等电子体,等电子体的结构相似、物理性质相似,根据等电子体的概念分析解答.
解答 解:阳离子NO2+与XO2分子原子总数相等,阳离子的价电子为5+6×2-1=16,XO2分子的价电子也是16,则X的价电子为16-6×2=4,位于第ⅣA族,可以是C或Si,但二氧化硅是原子晶体,不符题意,则X是C,故选C.
点评 本题考查等电子体的应用,明确等电子体的概念以及价电子的计算是解本题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列各组内的物质,按单质、化合物、混合物的顺序排列正确的是( )
| A. | 固态氨,矿泉水,漂粉精 | B. | 液态氧,干冰,水玻璃 | ||
| C. | 稀有气体,氯化钾,铁矿石 | D. | 天然气,氧化汞,不锈钢 |
5.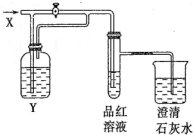 向如图所示的装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色.
向如图所示的装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色.
X和Y可能是 ( )
 向如图所示的装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色.
向如图所示的装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色.X和Y可能是 ( )
| 选项 | A | B | C | D |
| X | NO2 | SO2 | HCl | Cl2 |
| Y | 水 | 饱和NaHCO3溶液 | Na2SO3溶液 | Na2SO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
2. “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).下列有关该方法的叙述中正确的是( )
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).下列有关该方法的叙述中正确的是( )
 “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).下列有关该方法的叙述中正确的是( )
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).下列有关该方法的叙述中正确的是( )| A. | 该方法的一大缺点是能耗较大 | |
| B. | 整个过程中,只有一种物质可以循环利用 | |
| C. | 该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品 | |
| D. | “反应分离”环节中,分离物质的基本操作是蒸发、结晶、过滤 |
9.下列离子方程式错误的是( )
| A. | 氧化铁与稀硫酸反应:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 小苏打溶液中加入过量石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 硫酸与氯化钡反应:SO42-+Ba2+═BaSO4↓ | |
| D. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
19.下列变化中,不需要破坏化学键的是( )
| A. | 氯化氢气体溶于水 | B. | 碘升华 | ||
| C. | 加热氯酸钾使其分解 | D. | 氯化钠溶于水 |
3.下列有关表述正确的是( )
| A. | N原子的价电子轨道表示式: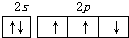 | |
| B. | 碳酸氢钠在水溶液中的电离方程式:NaHCO3?Na++H++CO32- | |
| C. | 羧基的结构式: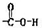 | |
| D. | 明矾的化学式为 KAlSO4•12H2O |


 .
.