题目内容
【题目】铈、铬、锡虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
(1)二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要应用.CeO2在稀硫酸和H2O2的作用下可生成Ce3+ , CeO2在该反应中作剂.
(2)自然界铬(Cr)主要以+3价和+6价存在.+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬.完成并配平下列离子方程式:
Cr2O72﹣+SO32﹣+═Cr3++SO42﹣+H2O
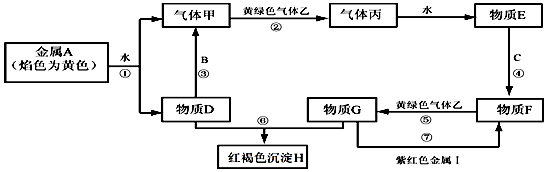
(3)实验室配制SnCl2溶液时往往因为生成Sn(OH)Cl而变浑浊,该过程的化学反应方程式为 . 氯气与金属锡在加热时可制得SnCl4 , SnCl4的熔点为﹣33℃,沸点为114℃,SnCl4极易水解,在潮湿的空气中有发烟现象.实验室可以通过如图所示装置制备SnCl4(夹持装置略). 
①装置Ⅰ中发生反应的离子方程式为 .
②装置Ⅱ中的最佳试剂为 , 装置Ⅶ的作用为 .
③Ⅳ中加热的作用之一是促进氯气与锡粉反应,加热的另一作用为 .
④为测定实验中所用锡粉的纯度(杂质不参与下列反应):取质量为m g的锡粉溶于足量稀硫酸中,向生成的SnSO4溶液中加入过量的Fe2(SO4)3溶液,用物质的量浓度为c molL﹣1的K2Cr2O7溶液滴定生成的Fe2+ , 共用去K2Cr2O7溶液的体积为V L,则锡粉中Sn的质量分数为(已知Fe3+可将Sn2+氧化为Sn4+ , 酸性环境下Cr2O72﹣可被还原为Cr3+).
【答案】
(1)氧化
(2)1;3;8H+;2;3;4
(3)SnCl2+H20?Sn(OH)Cl+HCl;MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;饱和氯化钠溶液;防止空气中水蒸气进入Ⅵ中,SnCl4水解;加热促进SnCl4气化,便于分离;
Mn2++Cl2↑+2H2O;饱和氯化钠溶液;防止空气中水蒸气进入Ⅵ中,SnCl4水解;加热促进SnCl4气化,便于分离;![]()
【解析】解:(1)CeO2在稀硫酸和H2O2的作用下可生成Ce3+ , Ce元素的化合价由+4价降低为+3价,则CeO2在反应中作氧化剂,所以答案是:氧化;(2)反应中Cr元素化合价由+6价降低到+3价,S元素化合价由+4价升高到+6价,则最小公倍数为12,由电子守恒和原子守恒、电荷守恒可知配平后的离子方程式为Cr2O72﹣+3SO32﹣+8H+═2Cr3++3SO42﹣+4H20,
所以答案是:1;3;8H+;2;3;4;(3)SnCl2在溶液中发生水解生成Sn(OH)Cl,其反应方程式为:SnCl2+H20Sn(OH)Cl+HCl;
所以答案是:SnCl2+H20Sn(OH)Cl+HCl;
由装置图可知装置Ⅰ应为制备氯气装置,涉及离子反应为MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O,装置Ⅱ为饱和食盐水,装置Ⅲ为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅳ中反应生成SnCl4 , 经冷却后在装置Ⅵ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅵ中,①装置Ⅰ中浓盐酸与MnO2在加热时发生反应产生氯气.发生反应的离子方程式为:MnO2+4H++2Cl﹣
Mn2++Cl2↑+2H2O,装置Ⅱ为饱和食盐水,装置Ⅲ为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅳ中反应生成SnCl4 , 经冷却后在装置Ⅵ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅵ中,①装置Ⅰ中浓盐酸与MnO2在加热时发生反应产生氯气.发生反应的离子方程式为:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O,
Mn2++Cl2↑+2H2O,
所以答案是:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;②由于盐酸有挥发性,所以在制取的氯气中含有杂质HCl,在与金属锡反应前要除去,因此装置Ⅱ中的最佳试剂为除去HCl同时还可以减少氯气消耗的饱和食盐水;SnCl4极易水解,在潮湿的空气中发烟.为了防止盐水解,所以要防止起水解.装置Ⅶ的作用为防止空气中的水蒸气进入Ⅵ中使SnCl4水解,
Mn2++Cl2↑+2H2O;②由于盐酸有挥发性,所以在制取的氯气中含有杂质HCl,在与金属锡反应前要除去,因此装置Ⅱ中的最佳试剂为除去HCl同时还可以减少氯气消耗的饱和食盐水;SnCl4极易水解,在潮湿的空气中发烟.为了防止盐水解,所以要防止起水解.装置Ⅶ的作用为防止空气中的水蒸气进入Ⅵ中使SnCl4水解,
所以答案是:饱和氯化钠溶液;防止空气中水蒸气进入Ⅵ中,SnCl4水解;③如果没有装置Ⅲ,则在氯气中含有水蒸汽,所以在Ⅳ中除生成SnCl4外,还会生成SnCl4水解产生的含锡的化合物Sn(OH)4或SnO2 , 加热促进SnCl4气化,便于分离,
所以答案是:加热促进SnCl4气化,便于分离;④令锡粉中锡的质量分数为x,则:
Sn | ~ | Sn2+ | ~ | 2Fe3+ | ~ | 2Fe2+ | ~ |
|
M g |
| |||||||
mx g | cV mol |
故 M g:mx g= ![]() mol:cV mol
mol:cV mol
解得x= ![]() ,
,
所以答案是: ![]() .
.

 期末集结号系列答案
期末集结号系列答案