题目内容
用0.1 mol/L NaOH溶液滴定0.1 mol/L盐酸,如达到滴定终点时不慎多加1滴NaOH溶液(1滴溶液体积约为0.05 mL),继续加水至50 mL,所得溶液的pH是( )
A.4 B.7.2
C.10 D.11.3
【答案】
C
【解析】试题分析:当两溶液恰好完全反应时,PH=7,但是恰好完全反应是,多加一滴NaOH溶液,那么C(OH-)=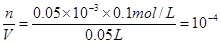 ,C(H+)=
,C(H+)=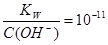 ,PH=
,PH=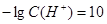
考点:酸碱滴定
点评:本道题难度适中,过量了0.05mL的NaOH,来计算PH值。

练习册系列答案
 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
下列图象表达正确的是( )
A、 如图表示25℃时,用0.1 mol?L-1的盐酸滴定20 mL 0.1 mol?L-1的NaOH溶液 | B、 如图表示常温下,两份足量、等浓度的盐酸与等量锌粉反应时,其中一份滴加了少量硫酸铜溶液 | C、 如图表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 | D、 如图表示适当升高稀硫酸的温度 |
下列图示与对应的叙述相符的是( )
A、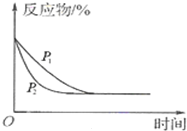 图表示压强对反应2A(g)+2B(g)═3C(g)+D(s)的影响,且P2>PI | B、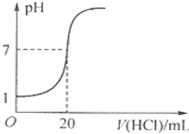 如图表示25℃时,用0.1 mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入盐酸体积的变化 | C、 依据如图,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4 | D、 图中开关K置于A或B处均可以减缓铁的腐蚀 |

 (2012?浙江模拟)下列说法正确的是( )
(2012?浙江模拟)下列说法正确的是( )