题目内容
下列图示与对应的叙述相符的是( )
A、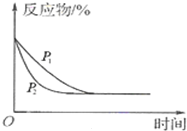 图表示压强对反应2A(g)+2B(g)═3C(g)+D(s)的影响,且P2>PI | B、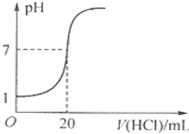 如图表示25℃时,用0.1 mol/L盐酸滴定20mL 0.1mol/L NaOH溶液,溶液的pH随加入盐酸体积的变化 | C、 依据如图,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4 | D、 图中开关K置于A或B处均可以减缓铁的腐蚀 |
分析:A、增大压强,化学反应速率加快,化学平衡向着气体系数和减小的方向进行;
B、20mL 0.1mol/L NaOH溶液的pH=13;
C、根据铁离子完全沉淀,铜离子不沉淀的pH数据来回答;
D、原电池的正极和电解池的阴极金属都是被保护的电极,据此回答判断.
B、20mL 0.1mol/L NaOH溶液的pH=13;
C、根据铁离子完全沉淀,铜离子不沉淀的pH数据来回答;
D、原电池的正极和电解池的阴极金属都是被保护的电极,据此回答判断.
解答:解:A、增大压强,化学反应速率加快,则P2>PI,加压平衡向着气体系数和减小的方向进行,即正向进行,所以P2条件下,反应物的含量小于P1条件下的,故A错误;
B、当盐酸的体积是0时,20mL 0.1mol/L NaOH溶液的pH=13,故B错误;
C、pH=4时,铁离子完全沉淀,铜离子不沉淀,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4,故C正确;
D、开关K置于A处,铁为阴极,被保护,但是当置于B处,铁为原电池的负极,被腐蚀,故D错误.
故选C.
B、当盐酸的体积是0时,20mL 0.1mol/L NaOH溶液的pH=13,故B错误;
C、pH=4时,铁离子完全沉淀,铜离子不沉淀,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4,故C正确;
D、开关K置于A处,铁为阴极,被保护,但是当置于B处,铁为原电池的负极,被腐蚀,故D错误.
故选C.
点评:本题综合考查影响化学反应速率的因素、酸碱中和滴定、除杂、电化学等方面的知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
下列图示与对应的叙述一定正确的是( )
A、图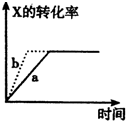 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 | B、图 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 | C、图 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 | D、图 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |


