题目内容
8.乙烯和苯是来自石油和煤的两种重要化工原料,特别是乙烯,其产量是衡量一个国家石油化工发展水平的标志.请回答:(1)下列物质中,不可以通过乙烯发生加成反应得到的是B(填序号)•
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D、CH3CH2Br
(2)工业上以乙烯为原料可以生产一种重要的合成有机髙分子化合物,该髙分子化合物结构简式为
 .
.(3)此外,乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一:

工艺二:
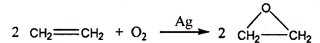
根据绿色化学的原则,理想的生产工艺是从源头上消除污染,充分利用参与反应的原理,使所有物质原料、中间产物都在内部循环、利用,实现零排放.因此,在实际生产中,应选择上述哪种工艺?工艺二(填“工艺一”或“工艺二”).
(4)苯也是一种重要的化工原料.苯的结构很特别,性质稳定.下列关于苯的叙述中不正确的是A.
A.常温下苯是一种无色无味的有毒气体
B.苯可以燃烧并伴有浓烈的黑烟
C.苯分子为平面正六边形结构
D、苯可与浓硝酸发生如下反应:

分析 (1)乙烯具有碳碳双键,性质较活泼,能和一些物质在一定条件下发生加成反应;
(2)乙烯能发生加聚反应生成聚乙烯;
(3)绿色化学为所有物质原料、中间产物都在内部循环、利用,实现零排放,根据绿色化学判断;
(4)A.常温下苯是一种无色有特殊气味的有毒液体;
B.苯的最简式为CH,含碳量较高;
C.苯分子中碳碳键都完全相同,所以其结构为平面正六边形;
D.在浓硫酸作催化剂、加热条件下,苯和浓硝酸发生取代反应生成硝基苯.
解答 解:(1)乙烯具有碳碳双键,性质较活泼,能和一些物质在一定条件下发生加成反应;
A.乙烯和氢气在一定条件下发生加成反应生成CH3CH3,故不选;
B.乙烯和氯化氢发生加成反应生成CH3CH2Cl而不是CH3CHCl2,故选;
C.乙烯和水发生加成反应生成CH3CH2OH,故不选;
D、乙烯和HBr发生加成反应生成CH3CH2Br,故不选;
故选B.
(2)乙烯能发生加聚反应生成聚乙烯,反应方程式为 ,故答案为:
,故答案为: ;
;
(3)绿色化学为所有物质原料、中间产物都在内部循环、利用,实现零排放,工艺一中有副产物生成,工艺二中没有副产物,所以工艺二符合绿色化学理念,故答案为:工艺二;
(4)A.常温下苯是一种无色有特殊气味的有毒液体,常作有机溶剂,故A错误;
B.苯的最简式为CH,含碳量较高,所以苯可以燃烧并伴有浓烈的黑烟,故B正确;
C.苯分子中碳碳键都完全相同,是一种介于单键和双键之间的特殊键,所以其结构为平面正六边形,故C正确;
D.在浓硫酸作催化剂、加热条件下,苯和浓硝酸发生取代反应生成硝基苯,反应方程式为 ,故D正确;
,故D正确;
故选A.
点评 本题考查常见有机物官能团及其结构,涉及苯的结构和性质、绿色化学、乙烯的结构和性质等知识点,结构决定性质,注意(1)中选项,无论乙烯发生加成反应还是取代反应都不能一步生成CH3CHCl2,题目难度不大.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案| A. | 利用天然气做燃料可以有效地减少“温室效应”的气体产生 | |
| B. | 由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分 | |
| C. | 可以用浸泡过高锰酸钾溶液的硅土来吸收水果或花朵产生的乙烯,达到保鲜目的 | |
| D. | 福尔马林是甲醛的水溶液,具有杀菌防腐能力,但不能用福尔马林保鲜鱼肉等食品 |
 英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些空洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织的“笼子”,整体上看呈现多孔特征,有些类似自然界中的蜂窝结构,下列有关说法正确的是( )
英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些空洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织的“笼子”,整体上看呈现多孔特征,有些类似自然界中的蜂窝结构,下列有关说法正确的是( )| A. | 该材料完全由金属元素构成 | |
| B. | 该材料能捕集CO2,是因为该材料可以选择性吸收CO2 | |
| C. | 该材料捕集11.2LCO2后,增重22g | |
| D. | 可利用该材料将空气中的CO2,完全捕集,从而控制温室效应 |
| A. |  | B. |  | C. |  | D. | 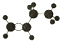 |
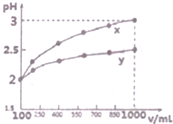 (1)现有浓度为0.1mol•-1的四种溶液①硫酸②醋酸③氢氧化钠④氯化铵.这四种溶液中由水电离出的H+浓度由大到小的顺序是④②③①(填序号).
(1)现有浓度为0.1mol•-1的四种溶液①硫酸②醋酸③氢氧化钠④氯化铵.这四种溶液中由水电离出的H+浓度由大到小的顺序是④②③①(填序号).
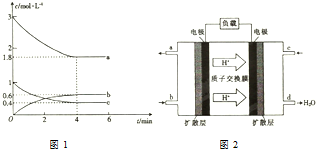 甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.
甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.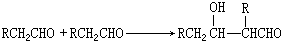
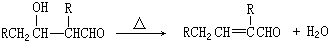
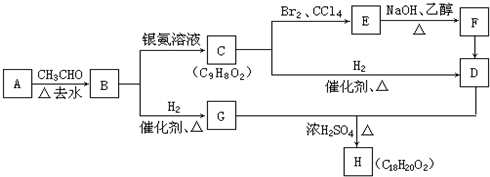
 ;
; +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$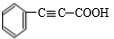 +2NaBr+2H2O
+2NaBr+2H2O +
+ $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$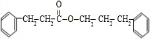 +H2O.
+H2O.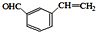 、
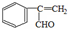
、 、
、
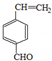 .
.