题目内容
18.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 0.6gCaCO3与Mg3N2的混合物所含质子数为0.3NA | |
| B. | 0.3mol/L的Na2SO4溶液中含有Na+和SO42-的总数目为0.9NA | |
| C. | 标准状况下,22.4LCCl4所含的氯原子数目为4NA | |
| D. | 1molNa2O2与足量的H2O完全反应时转移的电子数为2NA |
分析 A、CaCO3与Mg3N2的摩尔质量均为100g/mol,且两者中均含50个质子;
B、溶液体积不明确;
C、标况下四氯化碳为液体;
D、过氧化钠和水反应时,1mol过氧化钠转移1mol电子.
解答 解:A、CaCO3与Mg3N2的摩尔质量均为100g/mol,故0.6g混合物的物质的量为0.006mol,且两者中均含50个质子,故0.006mol混合物中含有的质子的物质的量为0.3mol,个数为0.3NA个,故A正确;
B、溶液体积不明确,故溶液中的离子的个数无法计算,故B错误;
C、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、过氧化钠和水反应时,1mol过氧化钠转移1mol电子,故转移NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
13.分枝酸可用于生化研究.其结构简式如图,下列关于分枝酸的叙述正确的是( )
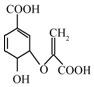

| A. | 分子式为C9H10O6 | |
| B. | 可与乙醇、乙酸反应,且反应类型相同 | |
| C. | 可使溴的四氧化碳溶液,酸性高锰酸钾溶液褪色,且原理相同 | |
| D. | 分子中含有三种官能团 |
3.下列叙述错误的是( )
| A. | 将少量CO2通入Na2SiO3溶液中会生成沉淀 | |
| B. | Li在氧气中充分燃烧,产物为Li2O | |
| C. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液呈红色 | |
| D. | 将过量的CO2气体通到NaAlO2溶液中可生成白色沉淀 |
10.下列反应不属于氧化还原反应的是( )
| A. | 3Fe+4H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 | |
| B. | 3NO2+H2O═2HNO3+NO | |
| C. | Ca(OH)2+SO2═CaSO3+H2O | |
| D. | Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O |
7.表是某地市场上销售的一种“加碘盐”包装袋上的部分文字说明.请根据此表结合初中学过的化学知识,回答下列问题:
(1)碘酸钾属于下列哪些类物质?(“纯净物”、“混合物”、“单质”、“化合物”、“酸”、“碱”、“盐”、“氧化物”)纯净物、盐
(2)根据含碘盐的食用方法,可推测碘酸钾的化学性质:碘酸钾在受热时易分解
(3)碘元素的最低化合价为-1,最高化合价为+7,则碘酸钾在氧化还原反应中能表现出的性质为即有氧化性又有还原性(填:“只有氧化性”、“只有还原性”、“即有氧化性又有还原性”)
| 配料表 | 精制海盐、碘酸钾(KIO3) |
| 含碘盐 | 20~40mg/kg |
| 储藏方法 | 密封避光、防潮 |
| 使用方法 | 烹调时待食品熟后加入碘盐 |
(2)根据含碘盐的食用方法,可推测碘酸钾的化学性质:碘酸钾在受热时易分解
(3)碘元素的最低化合价为-1,最高化合价为+7,则碘酸钾在氧化还原反应中能表现出的性质为即有氧化性又有还原性(填:“只有氧化性”、“只有还原性”、“即有氧化性又有还原性”)
 如图是一个电解过程示意图.假设使用N2H4-空气燃料电池作为本过程的电源,铜片质量变化128g,则N2H4一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)112L.
如图是一个电解过程示意图.假设使用N2H4-空气燃料电池作为本过程的电源,铜片质量变化128g,则N2H4一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)112L.