题目内容
19.下列说法中正确的是( )| A. | 金属元素和非金属元素交界处最容易找到制催化剂的材料 | |
| B. | 电能是现代社会中应用最广泛、最方便的一次能源 | |
| C. | 太阳能电池的主要材料是高纯度的二氧化硅 | |
| D. | 煤块粉碎为煤粉的目的是提高煤的燃烧效率 |
分析 A.在过渡元素区寻找催化剂;
B.电能不能在自然界直接获得;
C.Si为常见的半导体材料;
D.增大接触面积,反应速率加快.
解答 解:A.在过渡元素区寻找催化剂,则金属元素和非金属元素交界处最容易找到半导体材料,故A错误;
B.电能不能在自然界直接获得,则电能是现代社会中应用最广泛、最方便的二次能源,故B错误;
C.Si为常见的半导体材料,则太阳能电池的主要材料是高纯度的硅,故C错误;
D.增大接触面积,反应速率加快,则煤块粉碎为煤粉的目的是提高煤的燃烧效率,故D正确;
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、性质、反应速率等为解答的关键,侧重分析与应用能力的考查,注意元素周期表的指导作用,题目难度不大.

练习册系列答案
相关题目
10.一定条件下的反应N2(g)+3H2(g)?2NH3(g)达到化学平衡的本质原因是( )
| A. | 正、逆反应的速率相等且不为0 | B. | 反应体系中的气体压强保持不变 | ||
| C. | 正、逆反应都还在继续进行 | D. | 反应混合物中各组分的浓度相等 |
7.下列说法中不正确的是( )
| A. | 乙烯与苯都能使溴水褪色,但褪色原理不同 | |
| B. | 1mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol | |
| C. | 溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化还原反应 | |
| D. |  关系为同分异构体 关系为同分异构体 |
14.如图是锌铜原电池的示意图.下列关于锌铜原电池的说法中错误的是( )


| A. | 锌为负极.锏为正极 | |
| B. | 铜片上有大童气泡生成 | |
| C. | 电流由锌片经导线流向铜片 | |
| D. | 当反应过程中有0.2 mol电子发生转移时,生成了 2.24 L氢气 |
完成下列实验所需选择的装置或仪器都正确的是 ( )
| A | B | C | D |
实验 | 分离植物油和氯化钠溶液 | 除去氯化钠晶体中混有的硝酸钾晶体 | 分离CCl4中的I2 | 除去CO2气体中的HCl气体 |
装置 |
|
|
|
|
 如图为相互串联的甲乙两电解池.试回答:
如图为相互串联的甲乙两电解池.试回答: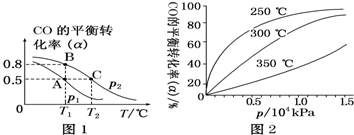 煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料.
煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料.