题目内容
13.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )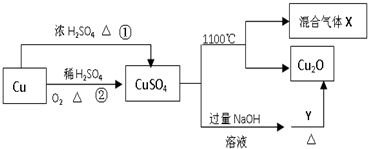
| A. | 途径①和途径②都体现了硫酸的酸性和氧化性 | |
| B. | 将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 | |
| C. | CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 | |
| D. | Y可以是酒精溶液 |
分析 A.根据反应物和生成物的化学式判断,途径①产生二氧化硫气体表现浓硫酸的氧化性,途径②是硫酸的酸性;
B、将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体;
C.硫酸铜分解生成Cu2O与氧气、SO2、SO3,依据电子守恒分析;
D.转化关系葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,蔗糖是非还原性糖不能和氢氧化铁反应生成氧化亚铜;
解答 解:A.途径①产生二氧化硫气体表现浓硫酸的氧化性,途径②是硫酸的酸性,无强氧化性,故A错误;
B.将CuSO4溶液蒸发浓缩、冷却结晶,过滤洗涤可制得胆矾晶体,故B正确;
C. 硫酸铜分解生成Cu2O与氧气、SO3、SO2,根据2CuSO4═Cu2O+SO2↑+SO3↑+O2↑知,X可能是O2、SO2和SO3的混合气体,若只是二氧化硫和三氧化硫,铜元素、氧元素化合价只有降低,无元素化合价升高,故C错误;
D.葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,蔗糖是非还原性糖不能和氢氧化铁反应生成氧化亚铜,不能使乙醇,故D错误,
故选B.
点评 本题考查了物质的制备,解题的关键是掌握物质的性质,解答时要依据题干提供信息,结合相关知识细心分析解答,题目难度中等.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
4.下列与标准状况下6.72L SO2气体含有氧原子数相同的是( )
| A. | 标准状况下6.72 L CO | B. | 0.3NA个Na2SO3 | ||
| C. | 常温常压下9.6g O2 | D. | 1.806×1023个H2O分子 |
1.下列说法中,正确的是( )
| A. |  与 与 互为同系物 互为同系物 | B. | 乙醇和二甲醚互为同分异构体 | ||
| C. | 乙醇、乙二醇、丙三醇互为同系物 | D. | 可用浓溴水来区分乙醇和苯酚 |
8.下列各组物质中,依次属于单质、酸、盐的一组是( )
| A. | 干冰、石灰石、氧化钙 | B. | 液氯、硝酸、纯碱 | ||
| C. | 水、烧碱、食盐 | D. | 氧气、盐酸、熟石灰 |
18.下列化学用语正确的是( )
| A. | 次氯酸分子的电子式: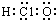 | B. | CH4Si的结构式: | ||
| C. | HCN分子的结构式:H-C≡N | D. | 丙烷分子的比例模型: |
5.NA代表阿伏加德罗常数的数值,下列有关NA的叙述中,正确的是( )
| A. | 1mol任何物质所含的分子数均为NA个 | |
| B. | 14 g氮气所含的N原子数为NA个 | |
| C. | 标准状况下,22.4 L SO3中所含分子数为NA个 | |
| D. | 在钠与氯气的反应中,1 mol氯气失去电子的数目为2NA个 |
2.根据如图的转化关系(反应条件已略去),判断下列说法正确的是( )

| A. | 反应①中氧化剂与还原剂的物质的量之比为1:4 | |
| B. | 反应②属于非氧化还原反应 | |
| C. | 相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1 | |
| D. | 根据反应⑤可判断还原性:Al>Mn |
3.下列说法正确的是( )
| A. | 明矾可用于水的消毒、杀菌 | B. | NaHCO3可用于治疗胃酸过多 | ||
| C. | 浓硝酸保存于无色玻璃瓶中 | D. | 氢氟酸可保存于玻璃瓶中 |
