题目内容
3.二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.下图是二甲醚、乙烷燃烧过程的能量变化图.请回答下列问题:(1)据图分析,a=$\frac{1}{3}$;
(2)当有3g乙烷完全燃烧时,可放出热量Q=156kJ.
(3)请根据该图写出1mol二甲醚完全燃烧的热化学方程式CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455kJ•mol-1.

分析 (1)依据原子守恒分析可知氢原子守恒,6a=2,a=$\frac{1}{3}$;
(2)图象分析可知$\frac{1}{3}$mol乙烷完全燃烧放热520KJ,结合定量关系计算3g乙烷完全燃烧时,可放出热量;
(3)图中是$\frac{1}{3}$mol二甲醚完全燃烧放热485KJ,结合热化学方程式书写方法标注物质聚集状态和对应反应的焓变写出.
解答 解:(1)图象中amol二甲醚燃烧生成水为1mol,依据原子守恒分析可知,氢原子守恒得到,6a=2,a=$\frac{1}{3}$,故答案为:$\frac{1}{3}$;
(2)图象分析可知$\frac{1}{3}$mol乙烷完全燃烧放热520KJ,结合定量关系计算3g乙烷完全燃烧时,放热=$\frac{3g}{30g/mol}$×520KJ×3=156KJ,故答案为:156 kJ;
(3)图中是$\frac{1}{3}$mol二甲醚完全燃烧放热485KJ,则1mol二甲醚完全燃烧放热=485KJ×3=1455KJ,反应的热化学方程式为:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455 kJ•mol-1,
故答案为:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455 kJ•mol-1.
点评 本题考查了热化学方程式书写方法,反应焓变的计算应用,图象分析判断,掌握基础是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.某强氧化剂XO(OH)2+,被亚硫酸钠还原到较低价态.如果还原2.4×10-3 mol XO(OH)2+,需用3mL 0.2mol/L的亚硫酸钠溶液,还原后X的最终化合价为( )
| A. | +3 | B. | +2 | C. | -2 | D. | +1 |
18.在一定温度下,反应:2A(s)+2B(g)?C(g)+D(g)在恒容的密闭容器中进行,能说明该反应已经达到平衡的是( )
| A. | 容器内的压强不随时间而变化 | |
| B. | B的正反应速率等于C的逆反应速率 | |
| C. | A的质量不再改变 | |
| D. | 单位时间内生成2a mol A,同时消耗a mol C |
15.法国化学家伊夫•肖万获2005年诺贝尔化学奖.他发现了烯烃里的碳-碳双键会被拆散、重组,形成新分子,这种过程被命名为烯烃复分解反应.烯烃复分解反应可形象地描述为交换舞伴.(如图所示)

烯烃复分解反应中的催化剂是金属卡宾(如CH2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈.随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴.后者会继续寻找下一个烯烃分子,再次“交换舞伴”.把C6H5CH2CH=CH2与CH2=M在一定条件下混合反应,下列产物不可能存在的是( )

烯烃复分解反应中的催化剂是金属卡宾(如CH2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈.随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴.后者会继续寻找下一个烯烃分子,再次“交换舞伴”.把C6H5CH2CH=CH2与CH2=M在一定条件下混合反应,下列产物不可能存在的是( )
| A. | C6H5CH2CH=M | B. | CH2=CH2 | ||
| C. | C6H5CH2CH2C6H5 | D. | C6H5CH2CH=CHCH2C6H5 |
12.某矿石样品中可能含铁,为确定其成分,进行如下操作:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 向溶液乙中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在Fe3+ | |
| B. | 向溶液乙中滴加少量氢氧化钠溶液,一定出现红褐色沉淀 | |
| C. | 向溶液甲中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在Fe3+ | |
| D. | 该矿石一定为赤铁矿 |
13.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )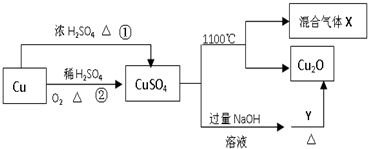

| A. | 途径①和途径②都体现了硫酸的酸性和氧化性 | |
| B. | 将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 | |
| C. | CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 | |
| D. | Y可以是酒精溶液 |


 .
.