题目内容
下列说法错误的是( )
| A、在1个CsCl晶胞中含有1个Cs+ |
| B、SO2在水中的溶解度比CO2在水中的溶解度要大 |
| C、X、Y元素同周期,且电负性X>Y,第一电离能可能Y大于X |
| D、根据电子排布的特点,Cu和Ga在周期表中都属于d 区 |
考点:不同晶体的结构微粒及微粒间作用力的区别,元素周期律的作用
专题:
分析:A.利用均摊法确定平均每个Csc1晶胞中有1个Cs+、1个C1-;
B.SO2属于极性分子,CO2属于非极性分子,根据相似相溶原理判断;
C.X、Y元素同周期,且电负性X>Y,则非金属性X>Y,一般非金属性强的,其第一电离能大,也有特殊情况;
D.Cu属于第IB族元素,Ga属于第IIIA主族.
B.SO2属于极性分子,CO2属于非极性分子,根据相似相溶原理判断;
C.X、Y元素同周期,且电负性X>Y,则非金属性X>Y,一般非金属性强的,其第一电离能大,也有特殊情况;
D.Cu属于第IB族元素,Ga属于第IIIA主族.
解答:
解:A.氯化铯晶体晶胞结构如图: ,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点,晶胞中铯离子个数=1,氯离子个数=
,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点,晶胞中铯离子个数=1,氯离子个数=
×8=1,故A正确;
B.SO2属于极性分子,CO2属于非极性分子,根据相似相溶原理极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂,水为极性溶剂,所以SO2在水中的溶解度比CO2在水中的溶解度要大,故B正确;
C.X、Y元素同周期,且电负性X>Y,则非金属性X>Y,一般非金属性强的,其第一电离能大,电负性X>Y,则第一电离能可能X>Y,特殊情况如最外层半充满或全充满结构的如:P的电负性小于S,但第一电离能P大于S,所以说可能Y>X,故C正确;
D.Cu属于第IB族元素,在周期表中位于ds区,Ga属于第IIIA主族,在周期表中位于p区,故D错误.
故选D.
 ,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点,晶胞中铯离子个数=1,氯离子个数=
,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点,晶胞中铯离子个数=1,氯离子个数=| 1 |
| 8 |
B.SO2属于极性分子,CO2属于非极性分子,根据相似相溶原理极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂,水为极性溶剂,所以SO2在水中的溶解度比CO2在水中的溶解度要大,故B正确;
C.X、Y元素同周期,且电负性X>Y,则非金属性X>Y,一般非金属性强的,其第一电离能大,电负性X>Y,则第一电离能可能X>Y,特殊情况如最外层半充满或全充满结构的如:P的电负性小于S,但第一电离能P大于S,所以说可能Y>X,故C正确;
D.Cu属于第IB族元素,在周期表中位于ds区,Ga属于第IIIA主族,在周期表中位于p区,故D错误.
故选D.
点评:本题考查了晶胞中微粒数目的计算、相似相溶原理、电负性和第一电离能、元素周期表的结构及应用等,题目涉及的知识点较多,侧重于基础知识的综合考查,题目难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
2013年1月28日日本岛发生火山喷发,将滚热的云状火山气体和火山灰喷向高空.火山气体主要包括①水蒸气②CO2③SO2④SO3⑤HCl,这些气体对环境造成了极大的危害,对①~⑤中的相关气体的叙述中不正确的是( )
| A、收集一定量的火山气体通入足量BaCl2溶液中,只能生成BaSO4一种沉淀 |
| B、②③④属于酸性氧化物 |
| C、⑤属于强电解质 |
| D、①②③④属于非电解质 |
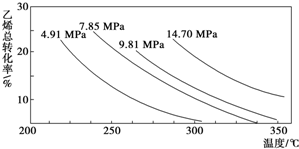 工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2═CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.如图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2═CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.如图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )| A、合成乙醇的反应一定为放热反应 |
| B、目前工业上采用250~300℃,主要是因为在此温度下乙烯的转化率最大 |
| C、目前工业上采用加压条件(7 MPa左右),目的是提高乙醇的产率和加快反应速率 |
| D、相同催化剂下,在300℃14.70 MPa乙醇产率反而比300℃7.85 MPa低得多,是因为加压平衡向逆反应方向移动 |
根据如表的数据,判断下列说法正确的是( )
| 离子化合物 | 离子电荷数 | 晶格能 kJ?mol-1 | 熔点 °C | 莫氏硬度 |
| NaF | 1 | 923 | 993 | 3.2 |
| NaCl | 1 | 786 | 801 | 2.5 |
| MgO | 2 | 3791 | 2852 | 6.5 |
| CaO | 2 | 3401 | 2614 | 4.5 |
| A、晶格能的大小与正负离子电荷数和距离成正比 |
| B、NaF晶体比NaCl晶体稳定 |
| C、表中物质CaO的晶体最稳定 |
| D、晶格能就是正负离子间的静电引力,晶格能越大,晶体的熔点越高,硬度越大 |
近年来我国大部分地区常被雾霾笼罩,PM2.5数据持续“爆表”,严重影响人们的身体健康.PM2.5是指大气中直径小于或等于2.5 μm(微米)的细小颗粒物,也称为可入肺颗粒物,它是大气的一种污染物,主要来自化石燃料的燃烧等.下列有关说法不正确的是( )
| A、“雾霾”不属于自然现象 |
| B、PM2.5的产生与人类活动有关 |
| C、PM2.5分散在空气中形成的混合物具有丁达尔效应 |
| D、开发利用新能源,减少化石燃料的使用是缓解雾霾天气发生的重要措施 |
下列事实不能用电化学原理解释的是( )
| A、铝片不需要特殊的保护方法 |
| B、炒过菜的铁锅未清洗易生锈 |
| C、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| D、镀锌铁比镀锡铁耐腐蚀 |