题目内容
13.在一定温度下的刚性密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s)+2B(g)?C(g)+D(g) 已达到平衡状态( )①混合气体的压强 ②混合气体的密度 ③各气体物质的物质的量浓度
④气体的总物质的量 ⑤混合气体的平均相对分子质量.
| A. | ②③⑤ | B. | ①②③ | C. | ②③④⑤ | D. | ①③④⑤ |
分析 可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变.
解答 解:该反应前后气体总物质的量不变,
①反应前后气体总物质的量不变,容器体积不变,则无论反应所带达到平衡状态混合气体的压强始终不变,不能据此判断平衡状态,故不选;
②反应前后气体总质量增大、容器体积不变,则混合气体的密度增大,当混合气体密度不变时该反应达到平衡状态,故选;
③反应前后各气体的物质的量改变,容器体积不变,则各气体的浓度发生变化,当各气体物质的物质的量浓度时,正逆反应速率相等,反应达到平衡状态,故选;
④反应前后气体的总物质的量不变,不能据此判断平衡状态,故不选;
⑤反应前后气体总质量增大、物质的量不变,所以混合气体平均相对分子质量增大,当混合气体的平均相对分子质量不变时,正逆反应速率相等,反应达到平衡状态,故选;
故选A.
点评 本题考查化学平衡状态判断,为高频考点,明确化学平衡状态判断方法及特点是解本题关键,侧重考查学生分析判断能力,注意该反应前后气体总质量改变且反应前后气体总物质的量不变,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列试剂中需要张贴图标志的是( )


| A. | HNO3 | B. | CuO | C. | NaCl | D. | C2H5OH |
1.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 100mL 1mol/LFeCl3溶液中含有0.1NA个Fe3+ | |
| B. | 1.06g Na2CO3含有的CO32-离子数小于0.01 NA | |
| C. | PH=3的醋酸溶液中,含有的H+数为0.001NA | |
| D. | 2L 0.5mol/L的氨水中,含有NH3•H2O、NH4+、NH3的总数为1 NA |
8.下列叙述正确的是( )
| A. | 标准状况下,1 mol任何物质体积均为22.4L | |
| B. | CH4的摩尔质量为16g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 1 mol H2O的质量为18g/mol |
5.下列说法中正确的是( )
| A. | 明矾的化学式为Al2(SO4)3•12H2O | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | AlCl3溶液与浓氨水反应有白色沉淀生成 | |
| D. | Al是重要的金属元素,其对应的氧化物为碱性氧化物 |
3.对于反应A2+3B2=2C来说,以下表示中,化学反应速率最快的是( )
| A. | v(B2)=0.8 mol/(L•s) | B. | v(A2)=0.3 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(B2)=0.9 mol/(L•s) |
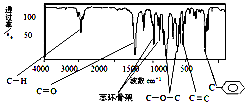
 (不考虑立体异构)
(不考虑立体异构)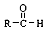 +CH3CHO$\stackrel{稀碱}{→}$
+CH3CHO$\stackrel{稀碱}{→}$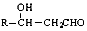 $\stackrel{-H_{2}O}{→}$RCH=CHCHO
$\stackrel{-H_{2}O}{→}$RCH=CHCHO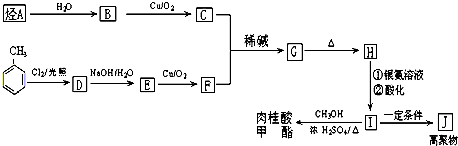

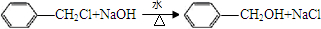
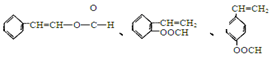
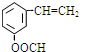 、
、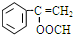 .
.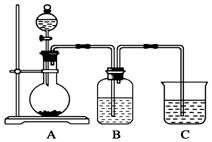 某同学设计实验以探究元素性质的递变规律,实验装置如图所示.
某同学设计实验以探究元素性质的递变规律,实验装置如图所示.