题目内容
配制0.5mol/L的NaOH溶液时,如果只存在下列问题,溶液的浓度如何变化?(填“偏高”、“偏低”、或“不变”).
(1)称量NaOH固体时,天平的砝码已锈蚀,其结果 .
(2)向容量瓶中加蒸馏水超过了刻度线后,又用滴管把多出的部分吸走,其结果 .
(1)称量NaOH固体时,天平的砝码已锈蚀,其结果
(2)向容量瓶中加蒸馏水超过了刻度线后,又用滴管把多出的部分吸走,其结果
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:根据C=
,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差.
| n |
| V |
解答:
解:(1)生锈的砝码质量偏大,而m物=m砝+m游,故称量出的药品的质量偏重,则配制出的溶液的浓度偏大,故答案为:偏高;
(2)向容量瓶中加蒸馏水超过了刻度线后,无法补救,必须重新配制,如果又用滴管把多出的部分吸走,则吸走的不止是水,也有溶质,会导致所配溶液的浓度偏低,故答案为:偏低.
(2)向容量瓶中加蒸馏水超过了刻度线后,无法补救,必须重新配制,如果又用滴管把多出的部分吸走,则吸走的不止是水,也有溶质,会导致所配溶液的浓度偏低,故答案为:偏低.
点评:本题考查了配制一定物质的量浓度溶液时的误差分析,要从不当的操作对溶液的体积或溶质的质量的影响来着手分析,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
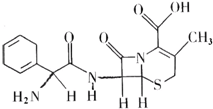 头孢拉定片(Cefradine Tablets),又称先锋霉素,该药品适宜敏感菌所导致的急性咽炎,扁桃体炎,中耳炎等呼吸道感染.其结构式如图所示,有关该物质的描述不正确的是( )
头孢拉定片(Cefradine Tablets),又称先锋霉素,该药品适宜敏感菌所导致的急性咽炎,扁桃体炎,中耳炎等呼吸道感染.其结构式如图所示,有关该物质的描述不正确的是( )| A、分子式为C16H20N3O4S |
| B、该物质在一定条件下能发生水解 |
| C、该有机物质不属于芳香族化合物 |
| D、该物质能与NaHCO3溶液反应放出CO2 |
实验室中配制一定物质的量浓度的Na2CO3溶液,必须使用的玻璃仪器是( )
A、 容量瓶 |
B、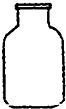 集气瓶 |
C、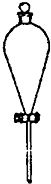 分液漏斗 |
D、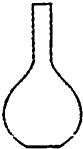 平底烧瓶 |
下列高分子材料所含成分相同的是( )①棉纤维 ②人造棉 ③人造丝 ④蚕丝 ⑤合成羊毛.
| A、①②③ | B、②③④ |
| C、④⑤ | D、全部 |
在25℃时,取PH均等于2的盐酸和醋酸溶液各100ml,先分别加水稀释至2 倍体积,再分别加入过量的锌粉.下列说法正确的是( )
| A、醋酸与锌反应放出氢气多 |
| B、两种酸放出氢气一样多 |
| C、醋酸与锌反应速率大 |
| D、两种酸与锌反应的速率一样大 |
有一种二肽化学式是C8H14N2O5,水解后得到丙氨酸和另一种氨基酸X,则X的化学式是( )
| A、C5H7N2O5 |
| B、C5H9N2O5 |
| C、C5H9NO4 |
| D、C5H11NO5 |
对于0.1mol?L-1Na2SO3溶液,下列说法正确的是( )
| A、降低温度,溶液的pH升高 |
| B、c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3) |
| C、c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-) |
| D、加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |