题目内容
实验室中配制一定物质的量浓度的Na2CO3溶液,必须使用的玻璃仪器是( )
A、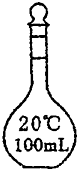 容量瓶 |
B、 集气瓶 |
C、 分液漏斗 |
D、 平底烧瓶 |
考点:不能加热的仪器及使用方法
专题:
分析:配制一定物质的量浓度的溶液一定用到容量瓶,根据图示选择容量瓶.
解答:
解:A.容量瓶,用此可配制100mL的一定浓度的溶液,故A正确;
B.集气瓶,用来收集气体或作物质在气体中燃烧实验,故B错误;
C.分液漏斗,用来分液或滴加液体,故C错误;
D.平底烧瓶用来制备气体所用,故D错误,
故选A.
B.集气瓶,用来收集气体或作物质在气体中燃烧实验,故B错误;
C.分液漏斗,用来分液或滴加液体,故C错误;
D.平底烧瓶用来制备气体所用,故D错误,
故选A.
点评:本题考查了常见仪器的用途,较简单,注意常见仪器的用途的知识的积累.

练习册系列答案
相关题目
可以用分液漏斗分离的一组混合物是( )
| A、苯和水 | B、酒精和碘 |
| C、醋酸和水 | D、碘和四氯化碳 |
FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)
已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )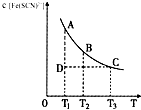
已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )

| A、其热化学方程式为:Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)△H>0 |
| B、温度为T1、T2时,化学反应速率分别为v1、v2,则v2<v1 |
| C、反应处于状态D时,一定有v正>v逆 |
| D、A点与B点相比,A点的c(Fe3+)大 |
下列实验能获得成功的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2;
②除去乙酸乙酯中少量的乙酸:加饱和Na2CO3溶液,充分振荡静置后,分液;
③除去CO2中少量的SO2;气体通过盛有饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的水:加新制生石灰,蒸馏.
⑤用溴水可鉴别苯、CCl4、苯乙烯;
⑥加浓溴水,然后过滤可除去苯中少量苯酚.
①除去乙烷中少量的乙烯:光照条件下通入Cl2;
②除去乙酸乙酯中少量的乙酸:加饱和Na2CO3溶液,充分振荡静置后,分液;
③除去CO2中少量的SO2;气体通过盛有饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的水:加新制生石灰,蒸馏.
⑤用溴水可鉴别苯、CCl4、苯乙烯;
⑥加浓溴水,然后过滤可除去苯中少量苯酚.
| A、②④⑤ | B、②③④ |
| C、①②④ | D、③④⑥ |
下列有关Ksp说法正确的是( )
| A、某温度下,CaSO4 溶液中C(Ca2+ )?C(SO42-) 就是 Ksp |
| B、25℃时,Fe(OH)3固体在0.01mol/LNH4Cl溶液中的溶解度增大,其Ksp也增大 |
| C、在一定条件下实现 BaSO4+Na2CO3?BaCO3+Na2SO4,说明KSP(BaSO4)>KSP(BaCO3) |
| D、升高温度,若某沉淀溶解平衡逆向移动,Ksp也变小 |
X、Y、Z、W四块金属分别用导线两两相连浸入稀硫酸中组成原电池,X、Y相连时,X为负极;Z、W相连时,电流方向是W→Z;X、Z相连时,Z极上产生大量气泡;W、Y相连时,W极发生氧化反应.据此判断金属的活动性顺序是( )
| A、Y>W>Z>X |
| B、X>Z>W>Y |
| C、Z>X>Y>W |
| D、X>Y>Z>W |
常温下,0.1mol?L-1某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、溶液中水电离出的c(H+)=10-10mol?L-1 |
| B、溶液中c(H+)+c(A-)=0.1 mol?L-1 |
| C、与0.05 mol?L-1NaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+) |
| D、上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液c(OH-)均增大 |