题目内容
18.在有机反应中能引入双键的反应是( )| A. | 磺化反应 | B. | 消去反应 | C. | 水解反应 | D. | 聚合反应 |
分析 有机物中,醇、卤代烃发生消去反应可生成双键,羟基氧化可生成醛基,三键加成和生成双键,以此解答该题.
解答 解:A.磺化反应为取代反应,不生成双键,故A不选;
B.消去反应可生成双键,如乙醇发生消去反应生成乙烯,故B选;
C.水解反应为取代反应,故C不选;
D.聚合反应生成高聚物,一般不生成双键,故D不选.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握常见有机反应类型与官能团的关系,难度不大.

练习册系列答案
相关题目
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 相同质量的N2和CO所含有的分子数、原子总数、电子总数都相等 | |
| B. | 50ml18.4 mol/L浓硫酸与足量铜加热反应,生成S02分子的数目为0.4 6 NA | |
| C. | 0.1mol/LMgCl2溶液中含有的Mg2+数目一定小于0.1NA | |
| D. | 1 mol CH5+中含有的电子数目为11NA |
6.下列有关NA的说法正确的是( )
| A. | 18g D2O和18g H2O中含有的质子数均为10NA | |
| B. | 2L 0.5 mol•L-1亚硫酸溶液中含有的H+离子数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 标准状况下,2.24L Cl2与过量的稀FeI2溶液反应,转移电子总数为0.1NA |
13.向NaCl、MgBr、KI 的混合溶液中通入一定量的Cl2后,若所得溶液中含有Br2,则一定不含有( )
| A. | Cl- | B. | Br- | C. | I- | D. | Cl2 |
3.设NA为阿伏伽德罗常数,下列说法错误的是( )
| A. | 1mol H2O所含电子数为10NA | |
| B. | 1mol Al与足量的稀盐酸溶液反应生成氢气1.5mol | |
| C. | 在标准状况下,0.5NA Cl2所占的体积约是11.2L | |
| D. | 在非标准状况下,22.4L O2含有的分子数一定不是NA |
10.氯碱工业是基础化学工业,在隔膜电解槽内电解氯化钠的饱和溶液可以得到H2,Cl2,NaOH,并由此形成氯碱产品系列.若将电解槽的内隔膜去掉,同时升高电解液的温度,此时电解产物间发生反应:Cl2+NaOH→NaClO3+NaCl+H2O (未配平),假设反应进行完全,则在该条件下最后得到的两种产物的物质的量之比是( )
| A. | 1:1 | B. | 1:2 | C. | 1:5 | D. | 2:3 |
14.X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大.有关信息如下表:
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式 .
.
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X>M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是PCl3+3H2O=3HCl+H3PO3.
(4)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
| X | 动植物生长不可缺少的元素,是组成蛋白质的重要元素 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
 .
.(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X>M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是PCl3+3H2O=3HCl+H3PO3.
(4)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
 $→_{过滤}^{调节PH_{3}-4}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O
$→_{过滤}^{调节PH_{3}-4}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O $\stackrel{40℃-50℃}{→}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O
$\stackrel{40℃-50℃}{→}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O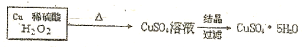 .
.