题目内容
钠、铝、铁是三种重要的金属,请回答:
(1)钠离子的结构示意图是
(2)三种金属中,既能与盐酸又能与氢氧化钠反应的是 (填化学式)写出其与氢氧化钠反应的化学方程式
(3)三种金属都能在一定条件下与水发生反应,写出铁与水蒸气发生反应的化学方程式
取一小块金属钠放在滴有酚酞的水中,实验现象是:钠浮在水面迅速反应、钠熔成小球并快速移动、反应中以听到嘶嘶的响声、 .
(1)钠离子的结构示意图是
(2)三种金属中,既能与盐酸又能与氢氧化钠反应的是
(3)三种金属都能在一定条件下与水发生反应,写出铁与水蒸气发生反应的化学方程式
取一小块金属钠放在滴有酚酞的水中,实验现象是:钠浮在水面迅速反应、钠熔成小球并快速移动、反应中以听到嘶嘶的响声、
考点:钠的化学性质,铝的化学性质,铁的化学性质
专题:
分析:(1)根据钠元素的离子核外电子层排布来解答;
(2)根据铝能和强酸、强碱反应;金属铝与氢氧化钠溶液反应生成了偏铝酸钠和氢气,据此写出反应的离子方程式;
(3)铁和水蒸气在高温下反应生成四氧化三铁和氢气;钠的密度小于水的密度,钠的熔点较低,钠和水反应生成氢气和氢氧化钠,同时有大量热量放出;
(2)根据铝能和强酸、强碱反应;金属铝与氢氧化钠溶液反应生成了偏铝酸钠和氢气,据此写出反应的离子方程式;
(3)铁和水蒸气在高温下反应生成四氧化三铁和氢气;钠的密度小于水的密度,钠的熔点较低,钠和水反应生成氢气和氢氧化钠,同时有大量热量放出;
解答:
解:(1)钠核外电子层排布可知:钠离子的结构示意图是 ;故答案为:
;故答案为: ;
;
(2)铝和强酸、强碱反应生成可溶性盐和氢气;铝与氢氧化钠溶液反应,反应生成偏铝酸钠和氢气,该离子反应为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑,
故答案为:Al;2Al+2H2O+2NaOH═2NaAlO2+3H2↑;
(3)高温下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为3Fe+4H2O(g)
Fe3O4+4H2;
钠的密度小于水的密度,所以钠会浮在水面上,钠的熔点较低,钠和水反应生成氢气和氢氧化钠,反应后的溶液变为红色
,同时有大量热量放出,放出的热量使钠熔成小球,生成的气体使钠受力不均,从而钠四处游动,并听到嘶嘶的响声;
故答案为:3Fe+4H2O(g)
Fe3O4+4H2;溶液变为红色;
 ;故答案为:
;故答案为: ;
;(2)铝和强酸、强碱反应生成可溶性盐和氢气;铝与氢氧化钠溶液反应,反应生成偏铝酸钠和氢气,该离子反应为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑,
故答案为:Al;2Al+2H2O+2NaOH═2NaAlO2+3H2↑;
(3)高温下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为3Fe+4H2O(g)
| ||
钠的密度小于水的密度,所以钠会浮在水面上,钠的熔点较低,钠和水反应生成氢气和氢氧化钠,反应后的溶液变为红色
,同时有大量热量放出,放出的热量使钠熔成小球,生成的气体使钠受力不均,从而钠四处游动,并听到嘶嘶的响声;
故答案为:3Fe+4H2O(g)
| ||
点评:本题考查了金属的反应,明确金属的性质是解本题关键,根据铝、钠、铁的性质分析解答,注意铁和水蒸气反应的生成物.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
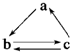 下列所列各组物质中,物质之间通过一步反应就能实现如图转化的是( )
下列所列各组物质中,物质之间通过一步反应就能实现如图转化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | CO2 | Na2CO3 | NaHCO3 |
| C | Si | SiO2 | H2SiO3 |
| D | CH2═CH2 | CH3CH2OH | CH3CHO |
| A、A | B、B | C、C | D、D |
将过氧化钠和过量的碳酸氢钠在密闭容器中混合充分加热后,最终残留固体物质是( )
| A、Na2CO3 |
| B、Na2O和Na2O2 |
| C、Na2O2 |
| D、Na2O2和Na2CO3 |
2009年5月12日汶川大地震一周年祭奠大会上,胡锦涛主席就灾后重建等相关问题发表了重要讲话.灾后重建需要大量钢材和金属合金材料,下列说法正确的是( )
| A、铁和钢材的主要化学成分相同,性质也相同 |
| B、硬铝(Al-Cu-Mg-Mn-Si合金)制成的门窗耐酸、耐碱、耐高温腐蚀 |
| C、黄铜矿(CuFeS2)可冶炼出Cu、Fe,同时可制取硫酸 |
| D、铁矿石是一种可再生资源,没有必要进行开采限制 |
为了保护臭氧层,可采取的有效措施是( )
| A、减少二氧化硫的排放 |
| B、减少卤代烃的排放 |
| C、减少废气的含铅量 |
| D、减少二氧化碳的排放 |
质量相同的乙烯和一氧化碳具有相同的( )
| A、物质的量 | B、原子个数 |
| C、体积和密度 | D、燃烧产物 |