题目内容
通过实验测定反应速率的方法有多种,如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的 来实现;在KMnO4与H2C2O4反应中,可通过测定 来测定该反应的速率;在Na2S2O3和H2SO4反应中,该反应的速率可通过 来测定.写出KMnO4与H2C2O4反应的离子方程式: .
考点:反应速率的定量表示方法,离子方程式的书写
专题:
分析:通过测定收集等体积H2需要的时间来测定锌粒与不同浓度硫酸反应时的速率;
KMnO4与H2C2O4发生氧化还原反应,生成锰离子、水和二氧化碳,反应后,溶液由紫红色变为无色,故可通过测定溶液褪色所需时间来测定该反应的速率;
Na2S2O3和H2SO4发生氧化还原反应,生成单质硫,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率.
KMnO4与H2C2O4发生氧化还原反应,生成锰离子、水和二氧化碳,反应后,溶液由紫红色变为无色,故可通过测定溶液褪色所需时间来测定该反应的速率;
Na2S2O3和H2SO4发生氧化还原反应,生成单质硫,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率.
解答:
解:通过实验测定反应速率的方法有多种,如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的时间来实现;
在KMnO4与H2C2O4反应中,反应后,溶液的紫红色颜色会消失,故可通过测定溶液褪色所需时间来测定该反应的速率;
在Na2S2O3和H2SO4反应中,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率;
KMnO4与H2C2O4发生氧化还原反应,生成锰离子、水和二氧化碳,离子方程式为:2MnO4-+5H2C2O4 +6H+=2Mn2++8H2O+10CO2↑,
故答案为:时间;溶液褪色所需时间;出现浑浊的时间;2MnO4-+5H2C2O4 +6H+=2Mn2++8H2O+10CO2↑.
在KMnO4与H2C2O4反应中,反应后,溶液的紫红色颜色会消失,故可通过测定溶液褪色所需时间来测定该反应的速率;
在Na2S2O3和H2SO4反应中,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率;
KMnO4与H2C2O4发生氧化还原反应,生成锰离子、水和二氧化碳,离子方程式为:2MnO4-+5H2C2O4 +6H+=2Mn2++8H2O+10CO2↑,
故答案为:时间;溶液褪色所需时间;出现浑浊的时间;2MnO4-+5H2C2O4 +6H+=2Mn2++8H2O+10CO2↑.
点评:本题考查反应速率的测定方法,难度不大.要注意通过实验测定反应速率的方法有多种,测定时间是其中的一种.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
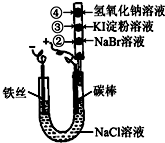 某化学兴趣小组按如图所示的装置进行实验,玻璃管内装有滴有不同溶液的白色棉球.实验过程中,两极均有气体生成.则下列说法错误的是( )
某化学兴趣小组按如图所示的装置进行实验,玻璃管内装有滴有不同溶液的白色棉球.实验过程中,两极均有气体生成.则下列说法错误的是( )| A、碳棒的电极反应式为2Cl--2e-=Cl2↑ | ||||
| B、②处、③处白色棉球分别变为橙黄色、蓝色 | ||||
C、如图X、Y两条线分别表示常见的非金属单质和金属单质(用M表示)与碳棒电解产物单质E在点燃条件下进行化合反应的物质的量之间的关系.写出符合Y线反应的化学方式Mg+Cl2
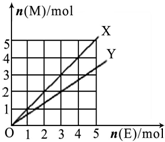 | ||||
| D、在20℃时饱和食盐水的质量分数为26%,当阳极析出1.12L(标准状况下)气体时,Cl-完全放电.试计算要使溶液恢复原状态,需加入3.65gHCl气体 |
氨硼烷(NH3BH3)是储氢量最高的化学氢化物储氢材料之一.室温下,NH3BH3是一种无色分子晶体,其可以与水发生催化脱氢反应:NH3BH3+2H2O
NH4BO2+3H2↑.少量氨硼烷可以由硼烷(B2H6)和NH3合成.下列有关说法正确的是( )
| 催化剂 |
| A、催化脱氢反应中NH3BH3作氧化剂 |
| B、NH4BO2和NH3BH3含有完全相同的化学键 |
| C、0.1 mol NH3BH3发生催化脱氢反应,可以生成6.72 L H2 |
| D、元素N的第一电离能高于相邻元素 |
最简单的烃,下列关于甲烷的叙述中不正确的是( )
| A、甲烷是烃类物质中相对分子质量最小的物质 |
| B、1molCH4在光照条件下最多能与4molCl2反应 |
| C、甲烷的二氯代物只有一种可以证明甲烷为正四面体结构 |
| D、甲烷与空气的体积比为1:2时,混合气点燃爆炸最剧烈 |
下列装置所示实验中,不能达到实验目的是( )
A、 制取少量氨气 |
B、 实验室制取氢氧化亚铁 |
C、 比较红磷和白磷的着火点 |
D、 实验室制取乙烯 |
NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| B、2.8gN2和2.24 LCO组成的混合物中质子数为1.4 NA |
| C、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4+ |
| D、25℃时,1LpH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA |
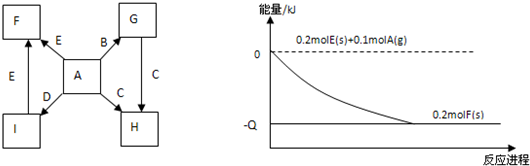
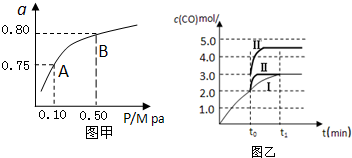
 工业上电解NO制备 NH4NO3,其工作原理如图所示,电解时阳极的电极反应为
工业上电解NO制备 NH4NO3,其工作原理如图所示,电解时阳极的电极反应为