题目内容
关于电解,下列叙述正确的是( )
| A、电解MgCl2饱和溶液,可制得金属镁 |
| B、电解NaCl溶液一段时间后,向阴极附近的溶液中滴入酚酞溶液,溶液呈无色 |
| C、若在铁表面镀锌,铁作阳极 |
| D、用电解法精炼铜时,粗铜作阳极 |
考点:电解原理
专题:电化学专题
分析:A、电解氯化镁溶液,在阴极上产生的是氢气,阳极上产生氯气;
B、电解氯化钠溶液,在阴极上产生的是氢气,该极附近氢离子浓度减小,氢氧根浓度增加,碱性增强;
C、电镀池中,镀件作阴极,镀层金属作阳极;
D、电解精炼铜时,粗铜作阳极,精铜是阴极.
B、电解氯化钠溶液,在阴极上产生的是氢气,该极附近氢离子浓度减小,氢氧根浓度增加,碱性增强;
C、电镀池中,镀件作阴极,镀层金属作阳极;
D、电解精炼铜时,粗铜作阳极,精铜是阴极.
解答:
解:A、电解氯化镁溶液,产物是氢氧化镁、氯气和氢气,故A错误;
B、电解氯化钠溶液,在阴极上产生的是氢气,该极附近氢离子浓度减小,氢氧根浓度增加,碱性增强,滴入酚酞溶液,溶液呈红色,故B错误;
C、电镀池中,镀件作阴极,镀层金属作阳极,在铁表面镀锌,锌作阳极,故C错误;
D、电解精炼铜时,粗铜作阳极,精铜是阴极,故D正确.
故选D.
B、电解氯化钠溶液,在阴极上产生的是氢气,该极附近氢离子浓度减小,氢氧根浓度增加,碱性增强,滴入酚酞溶液,溶液呈红色,故B错误;
C、电镀池中,镀件作阴极,镀层金属作阳极,在铁表面镀锌,锌作阳极,故C错误;
D、电解精炼铜时,粗铜作阳极,精铜是阴极,故D正确.
故选D.
点评:本题考查学生电解池的工作原理和应用知识,属于综合知识的考查,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )
| A、原子序数:X<Y |
| B、原子半径:X<Y |
| C、离子半径:X>Y |
| D、最外层电子数:X<Y |
用于净化汽车尾气的反应:2NO(g)+2CO(g)?2CO2(g)+N2(g),已知297℃时,该反应速率极慢,平衡常数为1×1059.下列说法正确的是( )
| A、提高尾气净化效率的最好方法是升高温度 |
| B、装有尾气净化装置的汽车排出的气体中一定不含NO或CO |
| C、297℃时该反应正向进行的程度很大,故使用催化剂并无实际意义 |
| D、提高尾气净化效率的最佳途径是研制高效催化剂 |
下列措施对增大反应速率明显有效的是( )
| A、在K2SO4与BaCl2两溶液反应时,增大压强 |
| B、Fe与稀硫酸反应制取H2时,改用浓硫酸 |
| C、Na与水反应时增大水的用量 |
| D、Al在氧气中燃烧生成A12O3,将Al片改成Al粉 |
下列各微粒的电子式正确的是( )
A、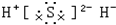 |
B、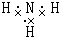 |
C、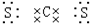 |
D、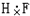 |
已知在比较酸的强弱时,必须考虑两方面:一是电离出氢离子的能力,二是溶剂接受氢离子的能力.比如HCl在水中是强酸,在冰醋酸中就是弱酸;而HAc在水中是弱酸,在液氨中却是强酸,就是因为接受氢离子的能力:NH3>H2O>HAc.下列关于酸性强弱的说法正确的是( )
| A、在A溶剂中,甲的酸性大于乙;在B的溶剂中,甲的酸性可能小于乙 |
| B、比较HCl、H2SO4、HClO4、HNO3酸性的强弱,用水肯定不可以,用冰醋酸可能可以 |
| C、HNO3在HClO4中是酸,在H2SO4中可能是碱 |
| D、比较HCN与HAc酸性的强弱,用水肯定可以,用液氨肯定也可以 |
下列有机物命名正确的是( )
A、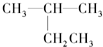 ,2-乙基丙烷 ,2-乙基丙烷 |
| B、(CH3)2CH-异丙基 |
C、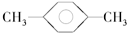 间二甲苯 间二甲苯 |
D、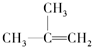 2-甲基-2-丙烯 2-甲基-2-丙烯 |
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).能判断该反应是否达到化学平衡状态的依据是( )
| A、容器中压强不变 |
| B、单位时间内消耗了n mol CO2,同时生成了n mol H2O |
| C、v正(H2)=v逆(H2O) |
| D、c(CO2)=c(CO) |