题目内容
在一密闭容器中充入NO2,在一定条件下进行反应:2NO2?2NO+O2.达到平衡状态的标志是( )
| A、NO2的消耗速率与NO的生成速率相等 |
| B、容器内压强不随时间变化而变化 |
| C、NO和O2的消耗速率之比为2:1 |
| D、单位时间内生成2n mol NO同时生成n mol O2 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:A.NO2的消耗速率是正反应速率,NO的生成速率也是正反应速率,故不能说明达到平衡状态,故A错误;
B.反应前后气体的体积不等,故容器内压强不随时间变化而变化可作为判断是否达到化学平衡状态的依据,故B正确;
C.反应速率之比等于化学计量数之比,故NO和O2的消耗速率之比为2:1不能作为判断是否达到化学平衡状态的依据,故C错误;
D.单位时间内生成2n mol NO是正反应速率,同时生成n mol O2也是正反应速率,故不能说明达到平衡状态,故D错误;
故选B.
B.反应前后气体的体积不等,故容器内压强不随时间变化而变化可作为判断是否达到化学平衡状态的依据,故B正确;
C.反应速率之比等于化学计量数之比,故NO和O2的消耗速率之比为2:1不能作为判断是否达到化学平衡状态的依据,故C错误;
D.单位时间内生成2n mol NO是正反应速率,同时生成n mol O2也是正反应速率,故不能说明达到平衡状态,故D错误;
故选B.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
下列物质无漂白作用的是( )
| A、氯水 | B、氨水 |
| C、二氧化硫 | D、次氯酸 |
化学在生活中无处不在,其中不科学的是( )
| A、含食品添加剂的食品都不属于绿色食品 |
| B、维生素C具有还原性,在人体内起抗氧化作用 |
| C、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
| D、地震后防疫人员在震区周围撒石灰,其作用是进行环境消毒,防止灾后出现疫情 |
在一定条件下,下列物质可与甲烷发生化学反应的是( )
| A、溴水 | B、氯水 |
| C、氧气 | D、高锰酸钾溶液 |
可逆反应aA(?)+2B(g)?2C(g)+D(g),其中a为正整数.反应中当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )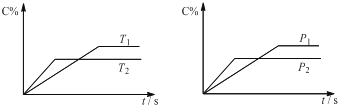

| A、达到平衡后,加入催化剂则C%增大 |
| B、达到平衡后,若升高温度,平衡正向移动 |
| C、a可以为任意的正整数 |
| D、达平衡后,增加A的量,有利于平衡正向移动 |
 某研究性学习小组的课题为“Mg、C原电池电解淀粉KI溶液的研究”,其研究装置如图所示.下列有关说法不正确的是( )
某研究性学习小组的课题为“Mg、C原电池电解淀粉KI溶液的研究”,其研究装置如图所示.下列有关说法不正确的是( )| A、镁为负极,发生氧化反应 |
| B、原电池中碳极反应式为Fe3++e-═Fe2+ |
| C、电解池中阴极处变蓝 |
| D、电解池中阴极处变红 |