题目内容
16.下列指定反应的离子方程式正确的是( )| A. | 将铜丝插入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 稀H2SO4与Ba(OH)2溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
分析 A.铜与稀硝酸反应,还原产物为一氧化氮;
B.电荷不守恒;
C.二者反应生成氢氧化铝沉淀和硫酸铵;
D.离子个数配比不符合物质结构.
解答 解:A.将铜丝插入稀硝酸中,离子方程式:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故A错误;
B.向Fe2(SO4)3溶液中加入过量铁粉,离子方程式:2Fe3++Fe═3Fe2+,故B错误;
C.向Al2(SO4)3溶液中加入过量氨水,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C正确;
D.稀H2SO4与Ba(OH)2溶液反应,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选:C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列物质分解后不留残渣的是( )
| A. | NaHCO3 | B. | NH4HCO3 | C. | KClO3 | D. | CaCO3 |
4.下列反应不属于氧化还原反应的是( )
| A. | 3Cl2+6KOH═5KCl+KClO3+3H2O | B. | 2NO2+2NaOH═NaNO3+NaNO2+H2O | ||
| C. | Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | D. | SnCl4+2H2O═SnO2+4HCl |
11.下列各组物质中,属于纯净物的是( )
| A. | 空气 | B. | 冰水混合物 | C. | 生理盐水 | D. | 雪碧饮料 |
1.下列反应的离子方程式书写不正确的是( )
| A. | 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+═BaSO4↓+NH3•H2O+H2O | |
| B. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+ClO═SO42-+Cl-+2H+ | |
| C. | 向Fe(NO3)3溶液中加入过量的HI溶液:Fe3++3NO3-+10I-+12H+═5I2+Fe2++3NO↑+6H2O | |
| D. | NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
8.把500mL有BaCl2和KCl的混合溶液分成2等份,一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 0.1(b-2a)mol/L | B. | 0.4( 2a-b)mol/L | C. | 10(b-2a)mol/L | D. | 4(b-2a)mol/L |
5.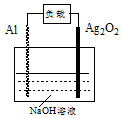 铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )
铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )
 铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )
铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )| A. | Ag2O2 为电池的正极 | B. | NaOH溶液为电解质溶液 | ||
| C. | 电池工作时,OH-向正极移动 | D. | 电池工作时,电能转变为化学能 |
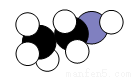
 氢能是一种极具发展潜力的清洁能源.
氢能是一种极具发展潜力的清洁能源.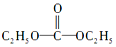 ,则碳酰肼的结构简式为
,则碳酰肼的结构简式为 .
.