题目内容
强酸与强碱的稀溶液发生中和反应的热效应为: H+(aq)+OH-(aq)===H2O(l) ΔH =-57.3kJ·mol-1。分别向1 L 0.5mol/L的NaOH溶液中加入①浓硫酸;②稀硫酸;③稀盐酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是( )
| A.ΔH1>ΔH2>ΔH3 | B.ΔH1<ΔH2<ΔH3 | C.ΔH1=ΔH2<ΔH3 | D.ΔH1<ΔH2=ΔH3 |
D
试题分析:根据中和热的定义强酸与强碱的稀溶液发生中和反应的热效应,故②、③相等。①浓硫酸溶于水形成稀溶液要放出热,故使得热效应变小。故D正确;

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
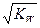
 2XY3(g) △H=-92.6 kJ·mol-1
2XY3(g) △H=-92.6 kJ·mol-1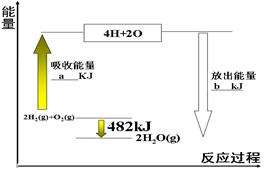

 Sn(白,s)ΔH3=+2.1 kJ·mol-1
Sn(白,s)ΔH3=+2.1 kJ·mol-1