题目内容
7.相同状况下混合下列同组气体,所得混合气体平均相对分子质量为36,它们可能是( )| A. | NO2和NO | B. | NO2和CO2 | C. | N2和O2 | D. | O2和CO |
分析 利用均值法,所得混合气体平均相对分子质量为36,其中一种相对分子量大于36,另一种小于36,由此分析解答.
解答 解:A、NO2的相对分子量为46大于36,NO的相对分子量为30小于36,所以混合气体的相对分子量可能为36,故A正确;
B、NO2和CO2的相对分子量分别为46和44,都大于36,不可能,故B错误;
C、N2和O2的相对分子量分别为28和32,都小于36,不可能,故C错误;
D、O2和CO的相对分子量分别为32和28,都小于36,不可能,故D错误;
故选A.
点评 本题考查平均相对分子量的有关计算,比较基础,注意均值法在解题中的灵活应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列溶液中微粒浓度关系正确的是( )
| A. | 含有NH4+、Cl-、H+、OH-的溶液中,离子浓度一定是c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 常温下,pH=6的醋酸与醋酸钠的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 将0.2 mol•L-1 CH3COOH溶液和0.1 mol•L-1 NaOH溶液等体积混合,则反应后的混合溶液中:2c(OH-)+c(CH3COO-)═2c(H+)+c(CH3COOH) | |
| D. | 常温下pH=6的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(NH3•H2O)>c(H+)>c(OH-) |
19.下列说法中有明显错误的是( )
| A. | 对有气体参加的化学反应,增大压强体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 | |
| B. | 升高温度,一般可使活化分子的百分数增大,因而反应速率增大 | |
| C. | 有效碰撞一定在活化分子之间,活化分子之间发生的碰撞一定为有效碰撞 | |
| D. | 加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率 |
16.化学与生产、生活、环境密切相关,下列说法中正确的是( )
| A. | 大力实施矿物燃料“脱硫、脱硝”技术,可减少酸雨的发生 | |
| B. | SiO2具有很好的导电性,可用于制取光导纤维 | |
| C. | 节日燃放的烟花,是碱金属、锶、铂、铁等金属化合物焰色反应所呈现的色彩 | |
| D. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
17.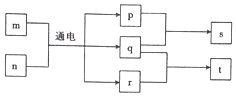 短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且Y、Z位于同一周期.m、n、s是由这些元素组成的二元化合物,p、q分别是W、Z两元素对应的单质,0.001mol•L-1s溶液的pH为3,t是混合溶液,且该溶液具有漂白性.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 元素Y分别与W、X、Z形成的化合物中一定含有离子键 | |
| B. | 离子半径:X<Y<Z | |
| C. | 由元素W、X组成的化合物中一定只含极性键 | |
| D. | s为强酸,r为弱碱 |