题目内容
某氮肥厂氨氮废水中的氮元素多以NH4+和NH3?H2O的形式存在,该废水的处理流程如图1所示:
过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收a.n
过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化示意图如图2:
(1)第一步反应是 反应(选填“放热”或“吸热”),判断依据是 .
(2)1mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 .

过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收a.n
过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化示意图如图2:
(1)第一步反应是
(2)1mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是

考点:"三废"处理与环境保护,热化学方程式
专题:化学应用
分析:(1)当反应物的总能量大于生成物的总能量,反应是放热的;
(2)结合图象根据盖斯定律来计算反应的焓变.
(2)结合图象根据盖斯定律来计算反应的焓变.
解答:
解:(1)焓变小于0,则反应为放热反应,故答案为:放热;因为△H=-273kJ/mol<0(反应物的总能量大于生成物的总能量);
(2)第一步的热化学方程式为NH4+(aq)+1.5O2(g)═NO2-(aq)+2H+(aq)+H2O(l),△H=-273KJ/mol,第二步的热化学方程式为:NO2-(aq)+0.5O2(g)═NO3-(aq),△H=-73KJ/mol,根据盖斯定律则NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol,
故答案为:NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol.
(2)第一步的热化学方程式为NH4+(aq)+1.5O2(g)═NO2-(aq)+2H+(aq)+H2O(l),△H=-273KJ/mol,第二步的热化学方程式为:NO2-(aq)+0.5O2(g)═NO3-(aq),△H=-73KJ/mol,根据盖斯定律则NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol,
故答案为:NH4+(aq)+2O2(g)═2H+(aq)+H2O(l)+NO3-(aq),△H=-346 kJ/mol.
点评:本题是一道有关热化学方程式的题目,关键抓住盖斯定律的应用,难度不大.

练习册系列答案
相关题目
下列有关物质性质或应用的说法正确的是( )
| A、蛋白质水解生成葡萄糖放出热量,提供生命活动的能量 |
| B、次氯酸钠具有强还原性,可用于配制消毒液 |
| C、氯气和二氧化硫都具有漂白性,两者混合使用能提高漂白的效率 |
| D、碳酸钠溶液显碱性,用热的饱和碳酸钠溶液可除去金属表面的油污 |
下列各组离子中,能在溶液中大量共存的是( )
| A、H+、Ca2+、Cl-、CO32- |
| B、I-、ClO-、K+、H+ |
| C、Na+、Fe3+、SO42-、OH- |
| D、Na+、Cu2+、Cl-、SO42- |
在AgNO3和Cu(NO3)2的混合溶液中,加入一定量的铁粉,充分反应后,有少量金属析出,过滤,向滤液中滴加盐酸,有白色沉淀生成,该沉淀不溶于稀硝酸,则析出的金属是( )
| A、Cu和 Ag |
| B、Ag |
| C、Cu |
| D、Cu 和 Fe |
常温时能与水反应产生H2 的是( )
| A、Na |
| B、NH4Cl |
| C、Na2O2 |
| D、NO2 |
下列气体不会造成空气污染的是( )
| A、NO |
| B、NO2 |
| C、N2 |
| D、SO2 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1 mol N2所含有的原子数为NA |
| B、标准状况下,22.4 L SO3中含有的分子数为NA |
| C、标准状况下,22.4 L氨气所含的原子数为NA |
| D、16 g O2和O3的混合气体所含的氧原子数为NA |
一种新型火箭燃料1,3,3-三硝基氮杂环丁烷(TNAZ)的结构如图所示.下列有关TNAZ的说法正确的是( )
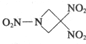

| A、分子中N、O间形成的共价键是非极性键 |
| B、该物质既有氧化性又有还原性 |
| C、C、N、O的第一电离能从大到小的顺序为O>N>C |
| D、C、N、0的气态氢化物的沸点依次降低 |