题目内容
11.己二酸是一种重要的有机二元酸,主要用于制造尼龙66纤维、尼龙66树脂和聚氨酯泡沫塑料.己二酸又名肥酸,白色晶体,微溶于水,易溶于醇、醚,可溶于丙酮,微溶于环己烷和苯.熔点153℃,沸点332.7℃,相对密度1.360.以环己酮(沸点155.6℃)为原料,在钨酸钠催化下,被双氧水氧化可得到己二酸.其反应方程式如下: +H2O2
+H2O2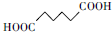 +H2O
+H2O
实验主要步骤如下
(Ⅰ)合成①将0.789g钨酸钠、0.32g磺基水杨酸和44mL 30%的过氧化氢水溶液加入如图1装置内,搅拌约15min.②加入10mL环己酮,在磁力加热搅拌器上缓慢加热至 90℃,回流恒温反应5h.③反应结束,将盛有物料的反应瓶冷却后置于冰水浴中静置3h,可见有大量晶体析出.
(Ⅱ)分离与提纯④待固体析出完全后,抽滤,用少量冰水洗涤,再抽干. ⑤将抽干得到的固体置于70℃的烘箱中干燥2.5h,即得粗产品.⑥粗产品经重结晶提纯得到精产品.重结晶过程加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥.回答下列问题
(1)若步骤③中固体析出不多,应采取的操作为将溶液加热浓缩至25~30mL,再冷却结晶.
(2)上述重结晶过程中的哪一步操作除去了不溶性杂质趁热过滤.
(3)己二酸重结晶的减压过滤装置如图2所示.
则仪器a的名称为布氏漏斗,装置B的作用是防止发生倒吸,装置C接在水龙头上,其作用是抽气,使吸滤瓶、安全瓶中的压强减小,减压过滤的操作有①将含晶体的溶液倒入漏斗;②将滤纸放入漏斗并用水湿润;③打开水龙头;④关闭水龙头;⑤拆下橡皮管.正确的顺序是②③①⑤④.
(4)己二酸纯度的测定准确称取试样0.12g于250mL锥形瓶中,加入50mL蒸馏水,稍加热,待其完全溶解后,加 2~3 滴酚酞指示剂,并用0.1mol•L-1 NaOH标准溶液滴定至终点(杂质不参与反应),此时溶液颜色由无色变为浅红色.滴定前后滴定管中的液面读数如图3所示,则该己二酸晶体样品中己二酸的质量分数为97.3%.
分析 以环己酮为原料在钨酸钠催化下,利用双氧水氧化可得到己二酸,涉及制备、分离提纯及产品分析,并对流程中操作的注意点及操作方法进行了讨论,可结合产品的性质,反应混合物的组成进行分析解答;
(1)只有饱和溶液里才有晶体析出,故步骤③从溶液里析出晶体时中析出不多,可考虑对反应混合液进行浓缩,促进晶体析出;
(2)当混合液里有多种溶质时可结合溶解度的差异进行重结晶,并选择趁热过滤,减少其它固体溶质析出,类似于用重结晶分离KNO3中混合有少量KCl;
(3)结合常见仪器可知仪器a为布氏漏斗,装置B为安全装置,可防倒吸,连接自来水可通过水流进行抽压,利于B装置的抽滤分离,可按正常操作顺序排序;
(4)滴定终点的分析可借助酚酞在己二酸溶液里的颜色与在氢氧化钠溶液里的颜色来分析,根据酸碱中和反应的原理,结合消耗的NaOH溶液的物质的量计算样品中含有的己二酸的物质的量,再计算纯度.
解答 解:(1)若步骤③中固体析出不多,应采取的操作为将溶液加热浓缩至25~30 mL,再冷却使晶体析出,故答案为:将溶液加热浓缩至25~30 mL,再冷却结晶;
(2)重结晶过程中的趁热过滤操作除去了不溶性杂质,故答案为:趁热过滤;
(3)仪器a的名称为布氏漏斗;装置B的作用是防止发生倒吸;装置C接在水龙头上起抽气作用,使吸滤瓶、安全瓶中的压强减小;减压过滤的正确操作顺序为②③①⑤④,故答案为:布氏漏斗;防止发生倒吸;抽气,使吸滤瓶、安全瓶中的压强减小;②③①⑤④;
(4)用0.1 mol•L-1的NaOH标准溶液滴定至终点时溶液颜色由无色变为浅红色,并在半分钟内不褪色;滴定时消耗NaOH溶液的体积为18.50-2.50=16.00(mL),NaOH的物质的量为0.1mol/L×0.016L=0.0016mol,己二酸的物质的量为0.0016mol÷2=0.0008mol,样品中己二酸的质量分数=$\frac{0.0008mol×146g/mol}{0.12g}$×100%=97.3%,故答案为:无色;浅红色;97.3%.
点评 本题利用氧化还反应原理进行物质制备,涉及混合物的分离提纯及纯度分析,综合性较强,通过练习对学生解题能力的培养有一定帮助,属中等难度.

 阅读快车系列答案
阅读快车系列答案| A. | 2 | B. | 7 | C. | 10 | D. | 12 |
| A. | 4:1 | B. | 1:4 | C. | 3:1 | D. | 1:3 |
请回答下列问题:
(1)根据反应原理,操作①所需的混酸溶液中硝酸和硫酸的理论配比(物质的量之比)为2:3.操作②中需要把NO与O2气体混合通入水中,混入该气体的目的是2NO+O2=2NO2、4NO2+O2+2H2O=4HNO3(用化学方程式表示).
(2)溶液I中存在一定浓度的Fe3+、Cu2+,在该浓度时生成氢氧化物沉淀的pH如右表.操作③中某学生设计物质X为H2O,若加水调整溶液pH,则Fe(OH)3开始沉淀的pH=1.9(填“<”、“>”或“=”);而实际操作中一般不用此法调节溶液pH,其主要原因是不利于蒸发浓缩.
| 开始沉淀 | 沉淀完全 | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
(4)为测定胆矾中结晶水的数目,称取25.0g胆矾品体在坩埚中加热,固体质量随温度升高而变化的曲线如图3.当固体质量为8.0g时,观察到固体完全呈黑色.请列式计算开始称取的胆矾中结晶水的数目.

I.已知反应 $\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)△H=-23.5kJ•mol-1,该反应在
1000℃的平衡常数等于4.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡.
(1)CO的平衡转化率=60%
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是d
a.提高反应温度 b.增大反应体系的压强 c.选取合适的催化剂
d.及时吸收或移出部分CO2e.粉碎矿石,使其与平衡混合气体充分接触
Ⅱ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题:

(3)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=0.15mol/(L•min)
(4)已知氢气的燃烧热286KJ/mol,请写出甲醇气体不充分燃烧的热化学方程式CH3OH(g)+O2(g)=2H2O(l)+CO(g)△H=-481kJ/mol.
(5)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
A.c1=c2B.2Q1=Q3C.2α1=α3D.α1+α2=1
E.该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量.
| ① | HF | Ka=6.8×10-4 mol•L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol•L-1 |
| ③ | HCN | Ka=6.2×10-10 mol•L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7 mol•L-1 Ka2=4.7×10-11 mol•L-1 |
(2)写出H2CO3的电离方程式H2CO3?HCO3-+H+、HCO3-?CO32-+H+;
(3)写出化学方程式:足量的氢氟酸与碳酸钠溶液混合2HF+Na2CO3═2NaF+H2O+CO2↑足量的CO2通入NaCN溶液中NaCN+H2O+CO2═HCN+NaHCO3.
 +
+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g的异戊醇、6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(3)本实验中加入过量乙酸的目的是提高醇的转化率.
(4)实验中加入少量无水MgSO4的目的是干燥乙酸异戊酯.
(5)在蒸馏操作中,图2中仪器选择及安装都正确的是b(填标号).

(6)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”),原因是会收集少量未反应的异戊醇.
(7)本实验的产率是c(填标号).a.30% b.40% c.60% d.90%

 .写出B的试管中所发生反应的化学方程式HBr+AgNO3=AgBr↓+HNO3.
.写出B的试管中所发生反应的化学方程式HBr+AgNO3=AgBr↓+HNO3.