题目内容
7.在一定条件下,可逆反应 N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol1,达到化学平衡状态时,下列说法正确的是( )| A. | 降低温度,可提高反应速率 | |
| B. | 加入合适的催化剂,可提高N2的转化率 | |
| C. | N2的正反应速率等于NH3的逆反应速率 | |
| D. | 反应物和生成物的浓度都不再发生变化 |
分析 A.降低温度,反应速率减小;
B.催化剂对平衡移动无影响;
C.平衡时不同物质的正逆反应速率之比等于化学计量数之比;
D.平衡时各组分的浓度不变.
解答 解:A.降低温度,反应速率减小,且该反应为放热反应,平衡正向移动,故A错误;
B.催化剂对平衡移动无影响,则不能提高转化率,故B错误;
C.平衡时不同物质的正逆反应速率之比等于化学计量数之比,则平衡时N2的正反应速率不等于NH3的逆反应速率,故C错误;
D.平衡时各组分的浓度不变,则平衡时反应物和生成物的浓度都不再发生变化,故D正确;
故选D.
点评 本题考查化学平衡,为高频考点,把握温度、浓度对平衡移动的影响、平衡判定为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.用NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 1L1mol•L-1KClO3溶液中含有的氯离子数目为NA | |
| B. | 22.4LH2含有的分子数目为NA | |
| C. | 等质量的C2H2与C6H6含有的原子总数相等 | |
| D. | 1molZn变为Zn2+时失去的电子数目为NA |
2.下列物质的水溶液因水解而呈酸性的是( )
| A. | NaCl | B. | MgCl2 | C. | NaHCO3 | D. | H2CO3 |
12.设NA为阿伏加德罗常数值,下列说法正确的是( )
| A. | 1 mol Cl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA | |
| B. | 将NA个NH3分子溶于1 L水中得到1 mol•L-1的氨水 | |
| C. | 标准状况下,22.4 L氮气与22.4 L苯所含分子数均为 NA | |
| D. | 常温常压下,32gO2、O3的混合物含有2NA个氧原子 |
7.茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案测定某品牌茶叶中钙元素的质量分数,并检验铁元素的存在(已知CaC2O4为白色沉淀物质).首先取200g茶叶样品焙烧得灰粉后进行如图操作:
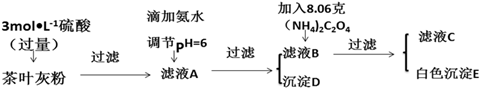
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的使样品中的有机物完全分解,将钙、铁等微量元素转化为可溶性物质.
(2)写出从滤液A→沉淀D的离子反应方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,判断D已经沉淀完全方法是静置,向上层清液中继续滴加氨水若无红褐色沉淀生成则说明D已沉淀完全,否则未沉淀完全.
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+═10CO2↑+2Mn2++8H2O.
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.

①此步操作过程中KMnO4标准溶液应装在图2中哪个仪器中(填写字母)B.
②滴定到终点,现象无色变为浅红色,静置后,如图3方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将偏高(填“偏高”“偏低”或“无影响”).
(5)原茶叶中钙元素的质量分数为0.3%.

请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 4.1 |
(2)写出从滤液A→沉淀D的离子反应方程式Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,判断D已经沉淀完全方法是静置,向上层清液中继续滴加氨水若无红褐色沉淀生成则说明D已沉淀完全,否则未沉淀完全.
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+═10CO2↑+2Mn2++8H2O.
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.

①此步操作过程中KMnO4标准溶液应装在图2中哪个仪器中(填写字母)B.
②滴定到终点,现象无色变为浅红色,静置后,如图3方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将偏高(填“偏高”“偏低”或“无影响”).
(5)原茶叶中钙元素的质量分数为0.3%.
5.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 100g质量分数为98%的浓硫酸中所含有的氧原子数为4NA | |
| B. | 足量的Fe与6.72LCl2反应转移的电子数为0.6NA | |
| C. | 密闭容器中1molN2与4molH2反应生成的NH3分子数小于2NA | |
| D. | 3g乙烷含有共用电子对为0.6NA |
 +CH2═CH-M$→_{碱}^{Pb}$
+CH2═CH-M$→_{碱}^{Pb}$ =CH-M+HX(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
=CH-M+HX(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下: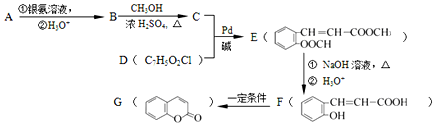
 .
. 中任意2种.
中任意2种. 的路线流程图:
的路线流程图: .
.