题目内容
15.用NA表示阿伏加德罗常数的值,下列判断正确的是( )| A. | 1L1mol•L-1KClO3溶液中含有的氯离子数目为NA | |
| B. | 22.4LH2含有的分子数目为NA | |
| C. | 等质量的C2H2与C6H6含有的原子总数相等 | |
| D. | 1molZn变为Zn2+时失去的电子数目为NA |
分析 A.1L 1mol/LKClO3溶液中不含有Cl-;
B.标况下,22.4LH2的物质的量为1mol,分子数目为NA;
C.C2H2和C6H6均可看成组分为(CH)n;
D.1molZn变为Zn2+时失去的电子数目为2NA.
解答 解:A.1L 1mol/LKClO3溶液中不含有Cl-,故A错误;
B.标况下,22.4LH2的物质的量为1mol,分子数目为NA,没有说标况,则无法确定物质的量,故B错误;
C.C2H2和C6H6均可看成组分为(CH)n,对于(CH)n,质量为mg时,物质的量为$\frac{m}{13n}mol$,含有的原子数为$\frac{m}{13n}×2n=\frac{2m}{13}mol$,可见,对于等质量的C2H2与C6H6含有的原子总数相等,故C正确;
D.1molZn变为Zn2+时失去的电子数目为2NA,故D错误.
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意气体摩尔体积的使用条件.

练习册系列答案
相关题目
6.A(g)+3B(g)?2C (g)△H=-b kJ•mol-1,一定条件下,在2L的恒容密闭容器中,反应30min,测得C的物质的量增加了6mol.下列说法正确的是( )
| A. | 第30min时,A的反应速率为0.05 mol•L-1•min-1 | |
| B. | 30min内,C的平均反应速率为0.02 mol•L-1•min-1 | |
| C. | 30min内,V(B)=$\frac{1}{3}$V(A) | |
| D. | 30min内,该反应放出的热量为3b kJ |
10.只用一种试剂就可以鉴别苯、碘化钾溶液、硝酸银溶液、己烯、四氯化碳,这种试剂是( )
| A. | NaOH溶液 | B. | Na2SO4溶液 | C. | 溴水 | D. | Na2CO3 |
20.下列仪器名称为“蒸馏烧瓶”的是( )
| A. |  | B. |  | C. | 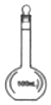 | D. |  |
7.在一定条件下,可逆反应 N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol1,达到化学平衡状态时,下列说法正确的是( )
| A. | 降低温度,可提高反应速率 | |
| B. | 加入合适的催化剂,可提高N2的转化率 | |
| C. | N2的正反应速率等于NH3的逆反应速率 | |
| D. | 反应物和生成物的浓度都不再发生变化 |
12.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 23 g钠的原子最外层电子数为2NA | |
| B. | 1 L 0.1 mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 标准状况下,22.4 L乙烷的分子数为NA | |
| D. | 1 mol甲基所含质子数为10NA |
13.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | B. |  和 和  互为同分异构体 互为同分异构体 | ||
| C. | 正丁烷和异丁烷是同系物 | D. |  和 和  是同一种物质 是同一种物质 |
