题目内容
13.下列操作能达到实验目的是( )| A. | 将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成 | |
| B. | 将溴乙烷与NaOH的乙醇溶液共热产生的气体通入溴水中,溶液褪色说明有乙烯生成 | |
| C. | 向稀氨水中滴加硝酸银溶液配得银氨溶液 | |
| D. | 溴乙烷与氢氧化钠溶液共热后,加入硝酸银溶液检验Br- |
分析 A.乙炔中混有硫化氢,具有还原性;
B.溴乙烷与NaOH的乙醇溶液共热产生,发生消去反应生成乙烯;
C.银氨溶液的配制:将氨水滴入硝酸银溶液中;
D.溴乙烷与氢氧化钠溶液共热后,发生水解反应生成溴离子,检验溴离子应在酸性溶液中.
解答 解:A.乙炔中混有硫化氢,具有还原性,则气体通入酸性KMnO4溶液中,溶液褪色不能说明有乙炔生成,故A错误;
B.溴乙烷与NaOH的乙醇溶液共热产生,发生消去反应生成乙烯,只有乙烯使溴水褪色,则溶液褪色说明有乙烯生成,故B正确;
C.银氨溶液的配制:将氨水滴入硝酸银溶液中且将生成的程度恰好溶解为止,故C错误;
D.溴乙烷与氢氧化钠溶液共热后,发生水解反应生成溴离子,检验溴离子应在酸性溶液中,则应先加硝酸至酸性再加入硝酸银溶液检验Br-,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的结构与性质、有机物检验等,把握有机反应及反应条件为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
6.已知汽车尾气无害化处理反应为2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0下列说法不正确的是( )
| A. | 升高温度可使该反应的逆反应速率降低 | |
| B. | 反应达平衡后,CO的反应速率保持不变 | |
| C. | 使用高效催化剂可有效提高正、逆反应速率 | |
| D. | 单位时间内消耗CO和N2的物质的量之比为2:1时,反应达到平衡 |
7.甲醛、乙醛、丙酸(C3H6O2)、丁烯、环氧乙烷(C2H4O)的混合物中,测得H的质量分数为9%,则混合物中O的质量分数为( )
| A. | 0.37 | B. | 0.24 | C. | 0.16 | D. | 无法确定 |
1.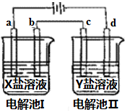 如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
 如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )| 选项 | X | Y |
| A | MgSO4 | CuSO4 |
| B | AgNO3 | KNO3 |
| C | FeSO4 | Al2(SO4)3 |
| D | CuSO4 | AgNO3 |
| A. | A | B. | B | C. | C | D. | D |
8.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )
| A. | 甲烷不能使酸性高锰酸钾溶液褪色,而甲苯能使酸性高锰酸钾溶液褪色 | |
| B. | 乙醇能发生消去反应,而乙烷不能发生消去反应 | |
| C. | 苯与硝酸在加热的条件下发生取代反应,而甲苯在常温下就能与硝酸发生硝化反应 | |
| D. | 乙烷在光照条件下能发生取代反应,而乙炔不能发生取代反应 |
18.下列离子方程式中,错误的是( )
| A. | 氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 在NaOH溶液中滴入几滴NH4Cl溶液:NH4++OH-═NH3•H2O | |
| C. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 将稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |