题目内容
11. A.B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去).
A.B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去).(1)若A为金属单质,D为某强酸的稀溶液,则A+B→C的离子方程式为Fe+2Fe3+=3Fe2+.
(2)若A、D均为非金属单质,则A+B→C的化学方程式为C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO.
(3)若A、B均为盐,A的水溶液显酸性,则A+B→C的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓.
分析 (1)若A为金属单质,D为某强酸的稀溶液,A和D反应的产物与D的量有关,且B和A反应生成C、C和D反应生成B,说明A为变价金属,为Fe,D为HNO3,则B为Fe(NO3)3、C为Fe(NO3)2;
(2)若A、D为非金属单质,B、C中有一种元素化合价不同,如果符合转化关系时,A为C、D为O2、C为CO、B为CO2;
(3)若A、B都为盐,A的水溶液呈酸性,为强酸弱碱盐,A和D的产物与D的量有关,A为AlCl3、D为NaOH、B为NaAlO2、C为Al(OH)3.
解答 解:(1)若A为金属单质,D为某强酸的稀溶液,A和D反应的产物与D的量有关,且B和A反应生成C、C和D反应生成B,说明A为变价金属,为Fe,D为HNO3,则B为Fe(NO3)3、C为Fe(NO3)2,则A和B生成C的离子方程式为Fe+2Fe3+=3Fe2+,
故答案为:Fe+2Fe3+=3Fe2+;
(2)若A、D为非金属单质,B、C中有一种元素化合价不同,如果符合转化关系时,A为C、D为O2、C为CO、B为CO2,则A和B生成C的化学方程式为C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,
故答案为:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;
(3)若A、B都为盐,A的水溶液呈酸性,为强酸弱碱盐,A和D的产物与D的量有关,A为AlCl3、D为NaOH、B为NaAlO2、C为Al(OH)3,则A和B生成C的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓.
点评 本题以Al、Fe、C元素及其化合物之间的转化为载体考查无机物推断,为高频考点,明确元素化合物性质及物质之间的转化是解本题关键,注意:有些化学反应产物与物质的量多少有关、有些与反应温度有关、有些与反应物浓度有关,注意基础知识点积累和灵活运用,题目难度中等.

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案| A. | m≥n | B. | 所得溶液中的溶质是NaAlO2、NaOH | ||
| C. | 固体是Al(OH)3 | D. | 固体是单质铝 |
| A. | 用碳棒连接电源的正极,另一电极用铜片 | |
| B. | 用铜片连接电源的正极,另一电极用铂片 | |
| C. | 阳极反应式为:Cu-2e═Cu2 | |
| D. | 阴极反应式为:2H++2e═H2↑ |
| A. | 蚁酸CH3COOH | B. | 石炭酸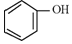 | C. | 氯仿CCl4 | D. | 甘油HOCH2CH2OH |
| A. | SO2→H2SO4 | B. | SiO2→H2SiO3 | C. | Al2O3→Al(OH)3 | D. | Fe2O3→Fe(OH)3 |
