题目内容
下列结论正确的是( )A.酸性:H2SO4>HClO4>H2SO3
B.酸性:HClO4>H2SO4>H2SO3
C.氢化物的稳定性:HF>HCl>H2S>H2Te
D.氢化物的稳定性:HF>H2S>HCl>H2Te
答案:BC
解析:
解析:
| 解析:根据“元素的非金属性越强,其相应的最高价氧化物的水化物的酸性越强,气态氢化物的稳定性越强”的知识解该题.S和Cl具有相同的电子层数,非金属性Cl>S,所以酸性HClO4>H2SO4.又因为H2SO4是强酸,H2SO3是中强酸,所以酸性H2SO4>H2SO3,则B项正确.F和Cl同周期,核电荷数F<Cl,非金属性F>Cl,S和Te相比,非金属性:S>Te,所以综合起来,非金属性:F>Cl>S>Te,则气态氢化物的稳定性:HF>HCl>H2S>H2Te.C项正确.
|

练习册系列答案
相关题目
己知:2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
| A、H2的燃烧热△H=-241.8kJ?mol-1 | B、炭和和水蒸气转化为水煤气为放热反应 | C、将24g 炭完全转化为水煤气,再充分燃烧,整个过程反应热为-787.0kJ?mol-1 | D、1mol H2O(g)完全分解需要吸收241.8kJ热量 |
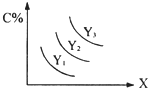 对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )
对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )| A、Y表示温度,X表示压强,且Y3>Y2>Y1 | B、Y表示压强,X表示温度,且Y3>Y2>Y1 | C、X表示压强,Y表示温度,且Y1>Y2>Y3 | D、X表示温度,Y表示压强,且Y1>Y2>Y3 |