题目内容
13.下列说法不正确的是( )| A. | 氯气可用于自来水的消毒 | B. | 二氧化硫可以用来漂白食品 | ||
| C. | 氢氧化铁胶体能用于净水 | D. | 镁可用于制造信号弹和焰火 |
分析 A.氯气溶于水生成HClO,根据HClO的性质分析;
B.二氧化硫具有漂白性,具有毒性;
C.氢氧化铁胶体表面积大,吸附能力强;
D.镁在空气中点燃,剧烈燃烧,发出耀眼的白光.
解答 解:A.氯气溶于水生成HClO,HClO具有强氧化性,可以杀菌消毒,故A正确;
B.二氧化硫具有漂白性,具有毒性,不可以用来漂白食品,故B错误;
C.氢氧化铁胶体表面积大,吸附能力强,能吸附水中的悬浮杂质,具有净水能力,故C正确;
D.镁在空气中点燃,剧烈燃烧,发出耀眼的白光,放出大量的热,生成白色固体氧化镁,镁是制造信号弹、焰火、闪光粉、轻质合金原料,故D正确;
故选B.
点评 本题考查了物质的性质和用途,题目难度不大,侧重于基础知识的考查,注意把握化学知识在生产生活中的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.在固定容积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g),已知反应过程某一时刻SO2、O2、SO3浓度分别为0.2mol•L-1、0.1mol•L-1、0.2mol•L-1,达到平衡时浓度可能正确的是( )
| A. | SO2为0.3 mol•L-1 | |
| B. | SO2、O2分别为0.4 mol•L-1、0.2 mol•L-1 | |
| C. | SO2、SO3均为0.25 mol•L-1 | |
| D. | SO2、SO3分别为0.24 mol•L-1、0.14 mol•L-1 |
4.下列元素中,最高正化合价数值最大的是( )
| A. | C | B. | Al | C. | S | D. | Ne |
1.下列溶液中跟100mL 0.1mol/L 硫酸钾溶液里钾离子物质的量浓度相同的是( )
| A. | 100 mL 0.2 mol/L 氯化钾溶液 | B. | 200 mL 0.1 mol/L 硝酸钾溶液 | ||
| C. | 100 mL 0.1 mol/L 硝酸钾溶液 | D. | 50 mL 0.2 mol/L 磷酸钾溶液 |
18.X(g)+3Y(g)?2Z(g)△H=-a kJ•mol-1,一定条件下,将1mol X和3mol Y通入2L的恒容密闭容器中,反应10min,测得Y的物质的量为2.4mol.X的平均反应速率是( )
| A. | 0.03 mol•L-1•s-1 | B. | 0.03 mol•L-1•min-1 | ||
| C. | 0.01 mol•L-1•s-1 | D. | 0.01 mol•L-1•min-1 |
3.下列变化会放出热量的是( )
| A. | 碘升华 | B. | 冰融化 | C. | 氯化铵溶于水 | D. | 氢氧化钠溶于水% |
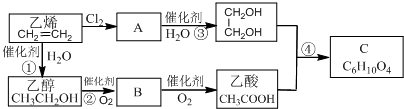
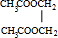 +2H2O.
+2H2O.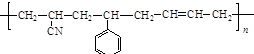 除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2.
除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2. )需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.
)需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.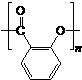 .
.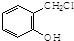 制备A的合成路线.
制备A的合成路线.