题目内容
17.下列说法正确的是( )| A. | 强电解质一定是离子化合物,弱电解质一定是共价化合物 | |
| B. | 强电解质一定是易溶化合物,弱电解质一定是难溶化合物 | |
| C. | SO3溶于水后水溶液导电性很强,所以SO3是强电解质 | |
| D. | 强电解质与弱电解质的本质区别是在水溶液中能否完全电离 |
分析 A.HCl是共价化合物、强电解质,氢氧化铝是弱电解质,但它是离子化合物;
B.强电解质和弱电解质的区别在于电离程度,与溶解度无关;
C.SO3溶于水自身不能发生电离,是非电解质;
D.根据强、弱电解质的定义分析.
解答 解:A.强电解质不一定是离子化合物,如HCl是共价化合物,但它在水溶液中能完全电离,它是强电解质,弱电解质也不一定是共价化合物,如氢氧化铝是弱电解质,但它是离子化合物,故A错误;
B.强电解质和弱电解质的区别在于电离程度,与溶解度无关,如硫酸钡是强电解质、醋酸是弱电解质,故B错误;
C.SO3溶于水自身不能发生电离,是非电解质,与水生成的亚硫酸是电解质,故C错误;
D.在水溶液中能够完全电离是强电解质,在水溶液中部分电离的是弱电解质,强电解质与弱电解质的本质区别是在水溶液中能否完全电离,故D正确;
故选D.
点评 本题考查了强、弱电解质的判断,抓住弱电解质的电离程度是解答本题的关键,题目难度不大,注意强电解质和弱电解质的区别在于电离程度,与溶解度无关.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
7.下列有关元素砷及其化合物的叙述中正确的是( )
| A. | 砷的第一电离能高于磷而电负性低于磷 | |
| B. | 三氯化砷与三氯化氮分子都是三角锥构型 | |
| C. | 最高氧化物对应水化物的化学式为HAsO3 | |
| D. | 砷的第一电离能小于同周期硒的电离能 |
8.下列实验装置图所示的实验操作,不能达到相应的实验目的是( )
| A. | 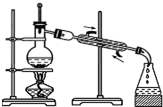 分离沸点相差较大液体混合物 | B. | 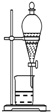 分离互不相溶的两种液体 | ||
| C. | 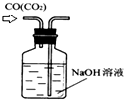 除去CO气体中的CO2气体 | D. | 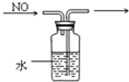 排水集气法收集NO |
5.工业上常利用Na2SO3溶液作为吸收液脱除硫酸工厂烟气中的SO2.下列说法正确的是( )
| A. | NaHSO3溶液中存在:c(Na+)>c(HSO3-)>c(OH-)>c(H+)>c(SO32-) | |
| B. | 当吸收液呈中性时:c(Na+)=2c(SO32-)+c(HSO3-) | |
| C. | 含等物质的量的Na2SO3和NaHSO3的溶液中,阴离子数目相等 | |
| D. | Na2SO3和NaHSO3都能抑制水的电离 |
2.下列属于电解质的是( )
| A. | 蔗糖 | B. | 硫酸铁溶液 | C. | 铜 | D. | 氢氧化钠 |
9.下列物质之间的转化都一步能实现的是( )
| A. | Si→SiO2→H2SiO3→Na2SiO3 | |
| B. | Al→Al2O3→Al(OH)3→NaAlO2 | |
| C. | Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3 | |
| D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
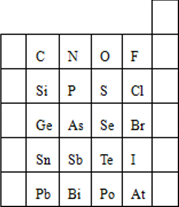 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.