题目内容
下列事实中,什么因素影响了化学反应速率
(1)黄铁矿煅烧时要粉碎成颗粒.
(2)熔化的KClO3放出旗袍很慢,撒入少量MnO2很快产生气体.
(3)夏天的食品易霉变,而冬天不易发生该现象.
(4)同样大小的石灰石分别在0.1mol/L盐酸和1mol/L的盐酸中反应速率不同
(5)同浓度同体积的盐酸放入大小相同的锌粒和镁条,产生气体有快有慢
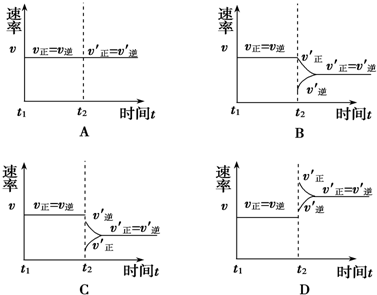
(6)恒温条件下,反应N2O4(g)═2NO2(g),将容器体积缩小一半 .
(1)黄铁矿煅烧时要粉碎成颗粒.
(2)熔化的KClO3放出旗袍很慢,撒入少量MnO2很快产生气体.
(3)夏天的食品易霉变,而冬天不易发生该现象.
(4)同样大小的石灰石分别在0.1mol/L盐酸和1mol/L的盐酸中反应速率不同
(5)同浓度同体积的盐酸放入大小相同的锌粒和镁条,产生气体有快有慢
(6)恒温条件下,反应N2O4(g)═2NO2(g),将容器体积缩小一半
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:常见影响反应速率的因素有浓度、温度、压强、催化剂等,一般来说,浓度越大、温度越高、压强越大,反应速率越大,加入催化剂,可增大反应速率,以此解答该题.
解答:
解:(1)黄铁矿煅烧时要粉碎成颗粒,固体表面积增大,反应速率增大,故答案为:固体表面积;
(2)MnO2起催化作用.即影响因素为催化剂,故答案为:催化剂;
(3)夏天气温高故食品易霉变,而冬天气温低不易发生该现象,即影响因素为温度,故答案为:温度;
(4)盐酸的浓度不同反应速率不同.即影响因素为浓度,故答案为:浓度;
(5)锌、镁的活泼性不同,与盐酸反应的速率不同,为物质的本身性质,故答案为:物质的本身性质;
(6)将容器体积缩小一半,压强增大,反应速率增大,故答案为:压强.
(2)MnO2起催化作用.即影响因素为催化剂,故答案为:催化剂;
(3)夏天气温高故食品易霉变,而冬天气温低不易发生该现象,即影响因素为温度,故答案为:温度;
(4)盐酸的浓度不同反应速率不同.即影响因素为浓度,故答案为:浓度;
(5)锌、镁的活泼性不同,与盐酸反应的速率不同,为物质的本身性质,故答案为:物质的本身性质;
(6)将容器体积缩小一半,压强增大,反应速率增大,故答案为:压强.
点评:本题考查化学反应速率的影响因素,难度不大,注意相关基础知识的积累,学习中要特别注意压强只对气体的反应速率有影响.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的产物中,一定能与KSCN溶液作用使溶液变红色的是( )
| A、铁与氯气 |
| B、铁与盐酸 |
| C、铁与氯化铁溶液 |
| D、铁与稀硝酸 |