题目内容
9.下列说法正确的是( )| A. | 18 g H2O在标准状况下的体积是22.4 L | |
| B. | 22.4 L O2中一定含有6.02×1023个氧分子 | |
| C. | 在标准状况时,20 mL NH3与60 mL N2所含的原子个数比为2:3 | |
| D. | 将80 g NaOH溶于1 L水中,所得溶液中NaOH的物质的量浓度为2 moL/L |
分析 A.H2O在标准状况下不是气体;
B.不是标准状况,无法计算;
C.根据n=$\frac{V}{Vm}$结合分子的组成分析;
D.溶液的体积不知,无法计算.
解答 解:A.H2O在标准状况下不是气体,不能用气体的摩尔体积计算,所以18 g H2O在标准状况下的体积不是22.4 L,故A错误;
B.不是标准状况,气体的摩尔体积的数值不知道,无法计算,故B错误;
C.由n=$\frac{V}{Vm}$可知,两种气体的物质的量分别为$\frac{0.02L}{22.4L/mol}$、$\frac{0.06L}{22.4L/mol}$,则原子的物质的量之比为$\frac{0.02L}{22.4L/mol}$×4:$\frac{0.06L}{22.4L/mol}$×2=2:3,故C正确;
D.将80 g NaOH溶于1 L水中,溶液的体积不是水的体积,所以溶液的体积不知,无法计算,故D 错误.
故选C.
点评 本题考查了气体摩尔体积的应用和溶液物质的量浓度的计算,题目难度不大,注意气体摩尔体积的适用条件.

练习册系列答案
相关题目
20.胶体区别于其它分散系最本质的特征是( )
| A. | 外观透明澄清 | B. | 分散质粒子直径介于1-100nm | ||
| C. | 静置,不出现分层 | D. | 有丁达尔现象 |
17.已知25℃下碳酸的电离常数K1=4.4×10-7,K2=4.7×10-11.下列有关碳酸溶液中各微粒浓度关系的说法正确的是( )
| A. | c(H+)═c(OH-)+c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$) | B. | c(H+)>c(HCO${\;}_{3}^{-}$)>c(H2CO3) | ||
| C. | c(H2CO3)═2c(H+)+c(CO${\;}_{3}^{2-}$) | D. | c(H+)═c(OH-)+c(HCO${\;}_{3}^{-}$)+c(CO${\;}_{3}^{2-}$) |
4.下列各组元素各项性质比较正确的是( )
| A. | 第一电离能:Li<Be<B | B. | 最高正价:O>N>C | ||
| C. | 电负性:O>C>Si | D. | 半径:K+>Cl- |
14.下列反应的离子方程式不正确的是( )
| A. | 铁与盐酸反应:2Fe+6H+=2Fe3++H2↑ | |
| B. | 氢氧化钠溶液与盐酸反应:OH-+H+=H2O | |
| C. | 锌与硫酸铜溶液反应:Zn+Cu2+=Zn2++Cu | |
| D. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
1.用激光柱照射下列分散系时,不能产生丁达尔效应的是( )
| A. | 石灰水 | B. | 稀豆浆 | C. | 云 | D. | Fe(OH)3胶体 |
18.根据表中信息判断,下列选项不正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-… | Cl2、Mn2+… |
| A. | 第①组反应的其余产物为H2O和 O2 | |
| B. | 第②组反应中Cl2与 FeBr2的物质的量之比为1:1 | |
| C. | 第③组反应中生成1mol Cl2,转移电子2mol | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Br2>Fe3+ |
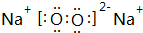 ;
; ,其原子核外有7个运动状态不同的电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃形.
,其原子核外有7个运动状态不同的电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃形.