题目内容
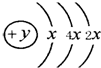 A、B、C、D四种短周期元素,且A、B、D为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图,据此填空:
A、B、C、D四种短周期元素,且A、B、D为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图,据此填空:(1)A的元素名称为
硅
硅
,其气态氢化物的化学式为SiH4
SiH4
.(2)A、B、C、D种元素的原子,半径由小到大的顺序为
O<S<P<Si
O<S<P<Si
.(3)分别画出B和D的原子结构示意图为



分析:A、B、C、D四种短周期元素,由A的电子排布可知,x=2,故A的电子排布2、8、4,故A为硅(Si)元素;C、B同主族,B、C可形成共价化合物BC3和BC2,可知B为S元素,C为O元素;A、B、D为相邻的同周期元素,故D为P元素.
解答:解:A、B、C、D四种短周期元素,由A的电子排布可知,x=2,故A的电子排布2、8、4,故A为硅(Si)元素;C、B同主族,B、C可形成共价化合物BC3和BC2,可知B为S元素,C为O元素;A、B、D为相邻的同周期元素,故D为P元素.
(1)由上述分析可知,A为硅元素,其气态氢化物的化学式为 SiH4.
故答案为:硅; SiH4.
(2)同周期自左而右,原子半径减小,故原子半径Si>P>S,同主族自上而下,原子半径增大,故原子半径S>O
,所以原子半径半径由小到大的顺序为O<S<P<Si.
故答案为:O<S<P<Si.
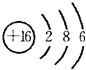
(3)B为S元素,原子核外有16个电子,有3个电子层,最外层电子数为6,原子结构示意图为 ;
;
D为P元素,原子核外有15个电子,有3个电子层,最外层电子数为5,原子结构示意图为 .
.
故答案为: ;
; .
.
(1)由上述分析可知,A为硅元素,其气态氢化物的化学式为 SiH4.
故答案为:硅; SiH4.
(2)同周期自左而右,原子半径减小,故原子半径Si>P>S,同主族自上而下,原子半径增大,故原子半径S>O
,所以原子半径半径由小到大的顺序为O<S<P<Si.
故答案为:O<S<P<Si.
(3)B为S元素,原子核外有16个电子,有3个电子层,最外层电子数为6,原子结构示意图为
 ;
;D为P元素,原子核外有15个电子,有3个电子层,最外层电子数为5,原子结构示意图为
 .
.故答案为:
 ;
; .
.点评:本题考查位置结构性质的相互关系、常用化学用语、半径比较等,题目难度中等,注意C、B同主族,二者可形成共价化合物BC3和BC2推断元素.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比3:4,D分别与A、B、C可形成10个电子的分子X、Y、Z.则下列叙述正确的是( )
| A、X、Y、Z三种分子的稳定性逐渐减弱 | B、上述四种元素共能形成五种单质 | C、X、Y、Z三种分子的沸点逐渐升高 | D、X、Y、Z三种分子均为极性分子 |

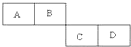 A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.