题目内容
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A、0.1mol?L-1 Na2CO3溶液中含有0.2NA个CO32- |
| B、常温下,23g NO2含有NA个氧原子 |
| C、1mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
| D、标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.明确告诉碳酸钠溶液的体积,无法计算溶液中碳酸根离子的数目;
B.23g二氧化碳的物质的量为0.5mol,含有1mol氧原子;
C.1mol双氧水完全被氧化成1mol铁离子失去了1mol电子;
D.标况下,四氯化碳的状态为液体,不能使用标况下的气体摩尔体积计算四氯化碳的物质的量.
B.23g二氧化碳的物质的量为0.5mol,含有1mol氧原子;
C.1mol双氧水完全被氧化成1mol铁离子失去了1mol电子;
D.标况下,四氯化碳的状态为液体,不能使用标况下的气体摩尔体积计算四氯化碳的物质的量.
解答:
解:A.题中缺少碳酸钠溶液的体积,无法计算溶液中碳酸根离子的物质的量及数目,故A错误;
B.23g二氧化碳的物质的量为0.5mol,0.5mol二氧化氮中含有1mol氧原子,含有NA个氧原子,故B正确;
C.1mol铁别氧化成1mol铁离子失去1mol电子,根据电子守恒,转移NA个电子,故C错误;
D.标准状况下,四氯化碳不是气体,题中条件无法计算5.6L四氯化碳的物质的量,故D错误;
故选B.
B.23g二氧化碳的物质的量为0.5mol,0.5mol二氧化氮中含有1mol氧原子,含有NA个氧原子,故B正确;
C.1mol铁别氧化成1mol铁离子失去1mol电子,根据电子守恒,转移NA个电子,故C错误;
D.标准状况下,四氯化碳不是气体,题中条件无法计算5.6L四氯化碳的物质的量,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下四氯化碳、乙醇、水等的状态不是气体,选项A为易错点,注意题中缺少溶液的体积.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
蓄电池在放电时起原电池作用,在充电时起电解池作用.下面是爱迪生蓄电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O
Fe(OH)2+Ni(OH)2.下列有关爱迪生蓄电池的说法正确的是( )
| 放电 |
| 充电 |
| A、放电时,Fe是负极,发生还原反应,NiO2是正极,发生氧化反应 |
| B、蓄电池的电极可以浸入某种酸性电解质溶液中 |
| C、放电时,电解质溶液中的阴离子向正极方向移动 |
| D、充电时,阴极上的电极反应式为:Fe(OH)2+2e-═Fe+2OH- |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1L 1mol?L-1的硫酸铝溶液中含有的Al3+为2NA |
| B、标准状况下,22.4L甲醇中含有的氧原子数为NA |
| C、1mol苯乙烯中含有的碳碳双键数为NA |
| D、4.2g C3H6中含有的碳碳双键数一定为0.1NA |
下列各图所示装置属于原电池的是( )
A、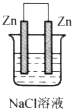 |
B、 |
C、 |
D、 |
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述不正确的是( )
A、NH4H的电子式为  |
B、NH4Cl的电子式为 |
| C、NH4H含有极性共价键和离子键 |
| D、NH4H固体投入少量热水中,有两种气体生成 |
下列离子方程式书写正确的是( )
| A、FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
| B、已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32- |
| C、AlCl3溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+2H2O+4NH4+ |
| D、等体积等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3?H2O+H2O |
以下命题,违背化学变化规律的是( )
| A、石墨制成金刚石 |
| B、水变成汽油 |
| C、用水制氢气 |
| D、酒变醋 |
生漆素有我国“三大宝”之誉,具有防腐蚀、耐强酸、耐强碱、防潮绝缘、耐高温等优良性能.漆酚是生漆的主要成分之一,其结构简式为 ,漆酚不具有的化学性质是( )
,漆酚不具有的化学性质是( )
 ,漆酚不具有的化学性质是( )
,漆酚不具有的化学性质是( )| A、可以与溴水发生取代、加成和氧化反应 |
| B、可以使酸性高锰酸钾溶液褪色 |
| C、可以跟FeCl3溶液发生显色反应 |
| D、可以跟Na2CO3溶液反应 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温常压下,0.1mol C8H18所含有的共价键数目为2.6NA |
| B、室温下,21.0g乙烯与丙烯的混合气体中含有的碳原子数为1.5NA |
| C、标准状况下,11.2L三氯甲烷所含分子数为0.5NA |
| D、0.1mol乙醇与氧化铜完全反应时转移电子数为0.1NA |