题目内容
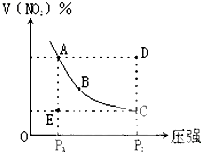 对于反应N2O4?2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).下列说法正确的是( )
对于反应N2O4?2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).下列说法正确的是( )| A、A、C两点的正反应速率的关系A>C |
| B、A、B、C、D、E各状态,V正<V逆的是状态E |
| C、维持P1不变,E→A所需时间为x,维持P2不变,D→C所需时间为y,则x<y |
| D、使E状态从水平方向到达C状态,从理论上来讲,可选用的条件是从P1突然加压至P2 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、根据压强对化学反应速率的影响分析,压强越大,反应速率越大;
B、处于曲线上的状态为平衡状态,在曲线以外的状态不处于平衡状态,根据从坐标的变化趋势判断反应进行的方向;
C、根据压强对化学反应速率的影响分析,压强越大,反应速率越大,达到平衡状态时用的时间越少;
D、从p1突然加压至p2,瞬间平衡没有移动,NO2的体积分数不变,再缓慢降压时,平衡向正反应方向移动,NO2的体积分数逐渐增大.
B、处于曲线上的状态为平衡状态,在曲线以外的状态不处于平衡状态,根据从坐标的变化趋势判断反应进行的方向;
C、根据压强对化学反应速率的影响分析,压强越大,反应速率越大,达到平衡状态时用的时间越少;
D、从p1突然加压至p2,瞬间平衡没有移动,NO2的体积分数不变,再缓慢降压时,平衡向正反应方向移动,NO2的体积分数逐渐增大.
解答:
解:A、增大压强,反应速率增大,C点压强大于A点压强,所以v(A)<v(C),故A错误;
B、处于曲线上的状态为平衡状态,E点NO2的物质的量少于平衡状态时的物质的量,反应应向生成NO2的方向移动,此时v(正)>v(逆),D点NO2的物质的量多于平衡状态时的物质的量,反应向逆反应方向移动,此时v(正)<v(逆),故B错误;
C、压强越大,反应速率越大,达到平衡状态时用的时间越少,E→A和D→C的物质的量相等,应为x>y,故C错误;
D、从p1突然加压至p2,瞬间平衡没有移动,NO2的体积分数不变,再缓慢降压时,平衡向正反应方向移动,NO2的体积分数逐渐增大,故D正确.
故选D.
B、处于曲线上的状态为平衡状态,E点NO2的物质的量少于平衡状态时的物质的量,反应应向生成NO2的方向移动,此时v(正)>v(逆),D点NO2的物质的量多于平衡状态时的物质的量,反应向逆反应方向移动,此时v(正)<v(逆),故B错误;
C、压强越大,反应速率越大,达到平衡状态时用的时间越少,E→A和D→C的物质的量相等,应为x>y,故C错误;
D、从p1突然加压至p2,瞬间平衡没有移动,NO2的体积分数不变,再缓慢降压时,平衡向正反应方向移动,NO2的体积分数逐渐增大,故D正确.
故选D.
点评:本题考查化学平衡移动图象问题,题目难度中等,本题注意把握曲线的含义,以此判断反应进行方向.

练习册系列答案
相关题目
下列实验操作合理的是( )
| A、中和滴定实验中的锥形瓶使用前应该用待装液洗涤 |
| B、用25 mL滴定管进行滴定实验时,消耗某溶液体积为21.70 mL |
| C、在托盘天平的托盘上各垫一张洁净的纸片直接称量NaOH固体 |
| D、用广泛pH试纸测得某溶液的pH为2.3 |
下列常用的干燥剂中,不能用来干燥氯气的是( )
| A、浓硫酸 |
| B、碱石灰 |
| C、无水氯化钙 |
| D、P2O5 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )


| A、反应开始到10s,用Z表示的反应速率为0.158mol/(L?s) |
| B、反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C、反应开始到10s时,Y转化了0.79mol |
| D、反应的化学方程式为:X(g)+Y(g)?Z(g) |
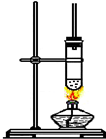 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反 应装置如图.下列对该实验的描述错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反 应装置如图.下列对该实验的描述错误的是( )| A、不能用水浴加热 |
| B、长玻璃管起冷凝回流作用 |
| C、提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
| D、浓硫酸的作用是催化剂和吸水剂 |
500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol?L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到11.2L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A、原混合溶液中c(K+)为4 mol?L-1 |
| B、上述电解过程中共转移1 mole- |
| C、电解得到的Cu的物质的量为1 mol |
| D、电解后溶液中c(H+)为4 mol?L-1 |
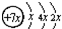 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: