题目内容
500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol?L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到11.2L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A、原混合溶液中c(K+)为4 mol?L-1 |
| B、上述电解过程中共转移1 mole- |
| C、电解得到的Cu的物质的量为1 mol |
| D、电解后溶液中c(H+)为4 mol?L-1 |
考点:电解原理
专题:电化学专题
分析:石墨作电极电解此溶液时,阳极发生的反应为:4OH-═2H2O+O2↑+4e-,
阴极上发生的电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,
两极均收集到11.2L(标况)气体,即均生成0.5mol的气体,阳极生成0.5mol氧气说明转移了2mol电子,而阴极上生成的0.5molH2只得到了1mol电子,所以剩余1mol电子由铜离子获得,且溶液中有0.5molCu2+,
再根据溶液为电中性,遵循电荷守恒可得钾离子物质的量浓度,从该溶液中析出Cu、H2、O2,
所以电解后加入一定量的Cu(OH)2可恢复为原溶液.
阴极上发生的电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,
两极均收集到11.2L(标况)气体,即均生成0.5mol的气体,阳极生成0.5mol氧气说明转移了2mol电子,而阴极上生成的0.5molH2只得到了1mol电子,所以剩余1mol电子由铜离子获得,且溶液中有0.5molCu2+,
再根据溶液为电中性,遵循电荷守恒可得钾离子物质的量浓度,从该溶液中析出Cu、H2、O2,
所以电解后加入一定量的Cu(OH)2可恢复为原溶液.
解答:
解:石墨作电极电解此溶液时,阳极发生的反应为:4OH-═2H2O+O2↑+4e-,
阴极上发生的电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,
两极均收集到11.2L(标况)气体,即均生成0.5mol的气体,阳极生成0.5mol氧气说明转移了2mol电子,而阴极上生成的0.5molH2只得到了1mol电子,所以剩余1mol电子由铜离子获得,且溶液中有0.5molCu2+,
A.c(Cu2+)=
=1mol/L,由电荷守恒可得c(K+)=6mol?L-1-1mol/L×2=4mol/L,故A正确;
B.由以上分析可知,述电解过程中共转移2 mole-,故B错误;
C.由以上分析可知,溶液中有0.5molCu2+,Cu2++2e-═Cu,所以电解得到的Cu的物质的量为0.5mol,故C错误;
D.电解后,c(K+)=4mol/L,c(NO3-)=6mol?L-1,则由电荷守恒可得c(H+)=6mol?L-1-4mol/L=2mol/L,故D错误;
故选A.
阴极上发生的电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,
两极均收集到11.2L(标况)气体,即均生成0.5mol的气体,阳极生成0.5mol氧气说明转移了2mol电子,而阴极上生成的0.5molH2只得到了1mol电子,所以剩余1mol电子由铜离子获得,且溶液中有0.5molCu2+,
A.c(Cu2+)=
| 0.5 |
| 0.5 |
B.由以上分析可知,述电解过程中共转移2 mole-,故B错误;
C.由以上分析可知,溶液中有0.5molCu2+,Cu2++2e-═Cu,所以电解得到的Cu的物质的量为0.5mol,故C错误;
D.电解后,c(K+)=4mol/L,c(NO3-)=6mol?L-1,则由电荷守恒可得c(H+)=6mol?L-1-4mol/L=2mol/L,故D错误;
故选A.
点评:本题考查电解池的工作原理以及溶液中的电荷守恒思想,明确离子的放电顺序及发生的电极反应是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
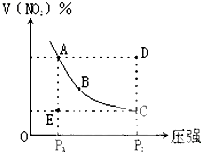 对于反应N2O4?2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).下列说法正确的是( )
对于反应N2O4?2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).下列说法正确的是( )| A、A、C两点的正反应速率的关系A>C |
| B、A、B、C、D、E各状态,V正<V逆的是状态E |
| C、维持P1不变,E→A所需时间为x,维持P2不变,D→C所需时间为y,则x<y |
| D、使E状态从水平方向到达C状态,从理论上来讲,可选用的条件是从P1突然加压至P2 |
配制200mL0.1mol/L稀硫酸时,下列实验操作使得所配溶液浓度偏小的是( )
| A、用量筒量取所需的浓硫酸时仰视读数 |
| B、定容后摇匀,发现液面最低点低于刻度线,再补加几滴蒸馏水至刻度线 |
| C、定容时,俯视刻度线 |
| D、未冷却至室温就进行后续操作 |
将一定量有机物充分燃烧后的产物通入足量石灰水中完全吸收,经过滤得到20g白色沉淀,滤液质量比原石灰水减少5.8g,该有机物是( )
| A、甲烷 | B、乙烯 |
| C、乙醇 | D、甲酸甲酯 |
下列操作正确的是( )
| A、给试管内的液体加热,可使试管口对准自己,不能使试管口对准别人 |
| B、用KMnO4制取O2时,先检验装置的气密性,然后再加药品 |
| C、把NaOH固体直接放在天平的左盘上称量 |
| D、稀释浓H2SO4时,可向盛浓H2SO4的量筒中小心加水 |
下列实验操作中,正确的是( )
| A、蒸发结晶时,应将溶液蒸干 |
| B、蒸馏中,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
| D、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释至刻度线 |
下列关于有机物的说法中,正确的一组是( )
①溴乙烷、乙酸乙酯在一定的条件下都能发生水解反应
②“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
③乙烯能使高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色,但褪色的原理不同
④石油的分馏、裂化和煤的干馏都是化学变化.
①溴乙烷、乙酸乙酯在一定的条件下都能发生水解反应
②“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
③乙烯能使高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色,但褪色的原理不同
④石油的分馏、裂化和煤的干馏都是化学变化.
| A、①③ | B、②④ | C、①② | D、③④ |
同样条件下,将Mg、Al、Fe分别投入质量相等且足量的稀H2SO4中,反应结束后三种溶液的质量相等,则投入Mg、Al、Fe的质量关系为( )
| A、Mg>Al>Fe |
| B、Mg<Al<Fe |
| C、Fe>Mg>AL |
| D、Fe<Mg<Al |