题目内容
2.如图表示4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合的.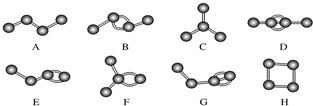
①图中分子式符合CnH2n+2的是AC(填字母).
②在如图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成碳碳双键和碳碳三键;不仅可以形成碳链,还可以形成碳环.
③图中互为同分异构体的是A与C;B与E、F、H(填字母).
④写出图中C物质的名称:2-甲基丙烷.
分析 (1)分子式符合CnH2n+2的是烷烃,而烷烃分子中,碳原子和其他原子均以单键成键;
(2)碳原子之间成键方式具有多样性,可以成碳链可以成碳环,可以形成双键、单键、三键;
(3)分子式相同而结构不同的有机化合物互为同分异构体,据此分析;
(4)C为烷烃,且主链上有3个碳原子,在2号碳原子上有一个甲基,据此分析.
解答 解:(1)分子式符合CnH2n+2的是烷烃,而烷烃分子中,碳原子和其他原子均以单键成键,根据图示的球棍模型可以看出,只有A、C中碳原子和其他原子以共价单键结合,属于烷烃,故答案为:AC;
(2)碳原子之间成键方式具有多样性,碳原子与碳原子之间不仅可以形成共价单键,还可以形成双键、三键,不仅可以形成碳链还可以形成碳环,
故答案为:碳碳双键;碳碳三键;碳链;
(3)分子式相同而结构不同的有机化合物互为同分异构体,A与C的分子式均为C4H10,而结构不同,故互为同分异构体;B与E、F、H的分子式均为C4H8,而结构不同,故互为同分异构体,故答案为:C;E、F、H;
(4)C为烷烃,且主链上有3个碳原子,在2号碳原子上有一个甲基,故名称为2-甲基丙烷,故答案为:2-甲基丙烷.
点评 本题考查学生球棍模型和同分异构体的知识,难度不大,注意结合题给信息“小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合”和图示分析.

练习册系列答案
相关题目
13.下列保存物质的方法正确的是( )
| A. | 液氯贮存在干燥的钢瓶里 | |
| B. | 少量的锂、钠、钾均保存在煤油中 | |
| C. | 氢氧化钠溶液保存在玻璃塞的细口瓶中 | |
| D. | 用排水法收集满一瓶氢气,瓶口朝上放置 |
10.下列混合物能用分液法分离的是( )
| A. | 乙醇与乙酸 | B. | 乙酸和水 | ||
| C. | 乙酸乙酯和Na2CO3溶液 | D. | 乙醇和水 |
17.在一含Na+的澄清溶液中,可能还存在NH4+、Fe2+、I-、Br-、CO32-、SO32-六种离子中的几种.
①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈橙黄色;
②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;
③橙黄色溶液不能使淀粉溶液变蓝色.
根据上述实验事实推断,下列说法不正确的是( )
①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈橙黄色;
②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;
③橙黄色溶液不能使淀粉溶液变蓝色.
根据上述实验事实推断,下列说法不正确的是( )
| A. | 溶液中一定存在Br-、CO32- | B. | 溶液中可能存在NH4+ | ||
| C. | 溶液中一定不存在Fe2+、I-、SO32- | D. | 溶液一定呈酸性 |
14.溶液、胶体和浊液这三种分散系的根本区别是( )
| A. | 是否是大量分子或离子的集合体 | B. | 是否均一、透明、稳定 | ||
| C. | 是否能透过滤纸或半透膜 | D. | 分散质微粒直径大小 |
11.不能用勒夏特列原理解释的是( )
| A. | 使用铁触媒,加快合成氨反应速率 | B. | 过量空气有利于SO2转化为SO3 | ||
| C. | 打开汽水瓶盖,即有大量气泡逸出 | D. | 配置FeCl3溶液时,加入少量盐酸 |
4.某溶液仅含 Fe2+?Na+?Al3+?Ba2+?SO42-?NO3-?Cl-中的4种离子,所含离子的物质的量均为1mol,若向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)?下列说法不正确的是
( )
( )
| A. | 该溶液中所含的离子是:Fe2+?Na+?SO42-?NO3-? | |
| B. | 若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色 | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 若向该溶液中加入足量的NaOH 溶液,充分反应后,过滤?洗涤?灼烧,最终所得固体的质量为72g |