题目内容
14.下列反应的离子方程式不正确的是( )| A. | 盐酸与氢氧化钠溶液反应:H++OH-═H2O | |
| B. | 铁丝与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| C. | 氯化亚铁溶液和氯气反应:Fe2++Cl2═Fe3++2Cl- | |
| D. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
分析 A.盐酸与氢氧化钠溶液反应生成氯化钠和水,实质为氢离子与氢氧根离子反应生成水;
B.铁丝与硫酸铜溶液发生置换反应生成硫酸亚铁和铜;
C.该离子方程式两边总电荷不相等,违反了电荷守恒;
D.氯化钡与稀硫酸反应实质为钡离子与硫酸根离子生成硫酸钡沉淀.
解答 解:A.盐酸与氢氧化钠溶液反应生成NaCl和水,反应的离子方程式为:H++OH-═H2O,故A正确;
B.铁丝与硫酸铜溶液反应生成硫酸亚铁和铜,反应的离子方程式为:Fe+Cu2+═Fe2++Cu,故B正确;
C.氯化亚铁溶液和氯气反应生成氯化铁,正确的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.氯化钡溶液与稀硫酸反应生成硫酸钡沉淀和氯化氢,反应的离子方程式为:Ba2++SO42-═BaSO4↓,故D正确;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
5.有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A→B;当A、C组成原电池时,A为正极;B与D构成原电池时,电极反应式为:D2++2e-═D,B-2e-=B2+.则A、B、C、D金属性由强到弱的顺序为( )
| A. | A>B>D>C | B. | A>B>C>D | C. | C>D>A>B | D. | C>A>B>D |
2.角膜接触镜俗称隐形眼镜,其性能要有良好的透气性和亲水性,目前大量使用的软性隐形眼镜常用材料是 ,下列有关该材料的说法不正确的是( )
,下列有关该材料的说法不正确的是( )
 ,下列有关该材料的说法不正确的是( )
,下列有关该材料的说法不正确的是( )| A. | 该材料是通过加聚反应得到的产物 | |
| B. | 该材料在一定条件下能发生水解反应 | |
| C. | 该材料的单体是 | |
| D. | 该材料分子的聚合度是n |
9.下列物质的类别与所含官能团都错误的是( )
| A. | 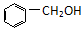 醇类-OH 醇类-OH | B. |  羧酸-COOH 羧酸-COOH | ||
| C. | 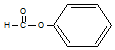 醛类-CHO 醛类-CHO | D. | CH3-O-CH3 醚类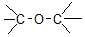 |
6.下列过程吸收热量的是( )
| A. | 氧化钙与水反应 | B. | 氮气液化 | C. | 碳酸钙分解 | D. | 浓硫酸稀释 |
3.在室温下,同种规格的镁条分别与下列物质混合,产生H2速率最快的是( )
| A. | 0.2mol/L的硫酸10mL | B. | 0.25mol/L的盐酸20mL | ||
| C. | 18.4mol/L的硫酸30mL | D. | 0.3mol/L的硝酸20mL |