题目内容
16.(1)硅酸钠的水溶液俗称水玻璃,向其中通入过量的CO2,会出现软而透明的凝胶胶体,其离子方程式是SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模转染性疾病暴发的有效方法之一.漂白粉是常用的消毒剂,工业上制漂白粉反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的有效成分是Ca(ClO)2(填化学式 )
(3)把Ba(OH)2溶液滴人明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是AlO2-,其离子反应方程式为Al3++4OH-+Ba2++SO42-=AlO2-+BaSO4↓+2H2O.
分析 (1)硅酸钠的水溶液俗称水玻璃,向其中通入过量的CO2,会出现软而透明的凝胶胶体硅酸胶体和碳酸氢钠;
(2)氯气在碱性条件下自身发生氧化还原反应,可与石灰乳反应生成氯化钙和次氯酸钙,次氯酸钙可生成具有氧化性的HOCl,可用于杀菌消毒;
(3)明矾的化学式为KAl(SO4)2•12H2O,设明矾为1mol,则溶液中含有1molAl3+,2molSO42-,根据反应:SO42-+Ba2+=BaSO4↓、Al3++4OH-=AlO2-+2H2O判断.
解答 解:(1)硅酸钠的水溶液俗称水玻璃,向其中通入过量的CO2,会出现软而透明的凝胶胶体硅酸胶体和碳酸氢钠,其离子方程式是SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-,故答案为:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;
(2)氯气与石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分为CaCl2和Ca(ClO)2,其中Ca(ClO)2可生成具有氧化性的HClO,可用于杀菌消毒,Ca(ClO)2为漂白粉的有效成分,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O; Ca(ClO)2;
(3)明矾的化学式为KAl(SO4)2•12H2O,设明矾为1mol,则溶液中含有1molAl3+,2molSO42-,由反应SO42-+Ba2+=BaSO4↓可知,使SO42-全部转化成BaSO4沉淀,需要2molBa(OH)2,则加入4molOH-,则发生Al3++4OH-=AlO2-+2H2O,所以最后溶液中存在AlO2-,反应的离子反应方程式为:Al3++4OH-+Ba2++SO42-=AlO2-+BaSO4↓+2H2O,
故答案为:AlO2-;Al3++4OH-+Ba2++SO42-=AlO2-+BaSO4↓+2H2O;
点评 本题考查酸性强弱的分析判断、漂白粉的有效成分和漂白原理、离子方程式的书写、离子反应定量关系,题目难度中等,注意判断使SO42-全部转化成BaSO4沉淀需要Ba(OH)2的物质的量,根据Al3+和OH-物质的量的关系判断反应产物.

 口算题天天练系列答案
口算题天天练系列答案| A. | 在蒸发皿中放入NaCl溶液,加热、蒸发得到NaCl晶体 | |
| B. | 用10 mL的量筒量取5.2 mL的盐酸 | |
| C. | 用托盘天平称取25.20 g NaCl | |
| D. | 用1 000 mL容量瓶配制450 mL 0.1 mol•L-1的盐酸 |
| A. | 在标准状况下,22.4L水所含分子数目为NA | |
| B. | 1mol•L-1 K2SO4溶液中所含K+数目为2NA | |
| C. | 1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为N A | |
| D. | O2的摩尔体积约为22.4 L•mol-1 |
| A. | Na2CO3俗称纯碱,属于盐类,可用于洗涤油污等 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
①氯气②液氯③新制氯水④敞口放置的久置氯水⑤盐酸⑥用盐酸酸化的漂白粉溶液.
| A. | ②③ | B. | ①②③④ | C. | ③⑥ | D. | ③④⑥ |
| A. | NaHCO3 | B. | NH4HCO3 | C. | KClO3 | D. | CaCO3 |
| A. | 空气 | B. | 冰水混合物 | C. | 生理盐水 | D. | 雪碧饮料 |
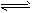 P(g)+Q(g),△H>0请回答下列问题:
P(g)+Q(g),△H>0请回答下列问题: