题目内容
5.下列操作中正确的是( )| A. | 过滤时,液面超过滤纸的边缘 | |
| B. | 加热试管内物质时,试管底部与酒精灯灯芯接触 | |
| C. | 过滤时,漏斗下端紧贴烧杯内壁 | |
| D. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 |
分析 A.过滤时液面应低于滤纸的边缘;
B.加热时用外焰加热;
C.过滤时,漏斗下端紧贴烧杯内壁,可防止液滴飞溅;
D.向试管中滴加液体时,应悬空正放.
解答 解:A.过滤时液面应低于滤纸的边缘,若液面超过滤纸的边缘,过滤失败,故A错误;
B.加热时外焰加热,不能试管底部与酒精灯灯芯接触,故B错误;
C.过滤时,漏斗下端紧贴烧杯内壁,可防止液滴飞溅,故C正确;
D.向试管中滴加液体时,应悬空正放,不能胶头滴管紧贴试管内壁,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验基本操作和实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
16.某化学兴趣小组设计如下流程,从酸性工业废液(含H+、Al3+、Mg2+、Cr3+、SO${\;}_{4}^{2-}$)中提取铬.

有关数据如表:
回答下列问题:
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是调节溶液的pH.
(2)若酸性废液中c(Mg2+)=0.lmol.L-l,为达到步骤①的实验目的,则废液的pH应保持在(5.3,7.8)范围(保留小数点后l位).
(3)步骤②中生成NaCrO2的离子方程式为Cr(OH)3+OH-=CrO2-+2H2O.
(4)步骤④中反应的离子方程式为7H2O+4CrO42-+6S=4Cr(OH)3↓+3S2O32-+2OH-.
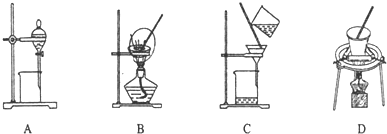
(5)步骤⑤在空气中充分灼烧的目的是使Cr(OH)3完全转化为Cr2O3,可选用的装置是D(填序号).
(6)用如图所示装置制取铬酸钠(Na2CrO4),回答相关问题.
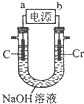
①a是电源的负极,阳极的电极反应式为Cr-6e-+8OH-=CrO42-+4H2O.
②若电解一段时间后阴极收集到标准状况下的气体3.36L,则理论上可制得8.1g铬酸钠(忽略反应2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)的影响)

有关数据如表:
| 化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| 完全沉淀的Ph | 10.5 | 4.3 | 5.3 |
| 开始溶解的pH | -- | 7.8 | 9.2 |
| Ksp近似值 | 10-12 | 10-14 | 10-31 |
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是调节溶液的pH.
(2)若酸性废液中c(Mg2+)=0.lmol.L-l,为达到步骤①的实验目的,则废液的pH应保持在(5.3,7.8)范围(保留小数点后l位).
(3)步骤②中生成NaCrO2的离子方程式为Cr(OH)3+OH-=CrO2-+2H2O.
(4)步骤④中反应的离子方程式为7H2O+4CrO42-+6S=4Cr(OH)3↓+3S2O32-+2OH-.
(5)步骤⑤在空气中充分灼烧的目的是使Cr(OH)3完全转化为Cr2O3,可选用的装置是D(填序号).

(6)用如图所示装置制取铬酸钠(Na2CrO4),回答相关问题.

①a是电源的负极,阳极的电极反应式为Cr-6e-+8OH-=CrO42-+4H2O.
②若电解一段时间后阴极收集到标准状况下的气体3.36L,则理论上可制得8.1g铬酸钠(忽略反应2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)的影响)
20.下列所陈述的事实与解释均正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 用pH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
| B | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
| C | 向某溶液中加入几滴新制的氯水,再加入2滴KSCN溶液,溶液变为红色 | 原溶液中一定含有Fe2+ |
| D | 甲苯能使酸性高锰酸钾溶液褪色 | 发生了萃取 |
| A. | A | B. | B | C. | C | D. | D |

 如图所示,甲、乙两池的电极材料都是铁棒与碳棒,丙池是电解精炼铜.
如图所示,甲、乙两池的电极材料都是铁棒与碳棒,丙池是电解精炼铜.