题目内容
10.已知:铅蓄电池总反应式为 Pb+PbO2+2H2SO4 $?_{充电}^{放电}$2H2O+2PbSO4;镍镉碱性充电电池在放电时,其电极反应为:正极:2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-
负极:Cd+2OH--2e-=Cd(OH)2
铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用,而镍镉电池使用一段时间后,其内阻几乎不变.请回答下列问题:
(1)写出铅蓄电池放电时负极的电极反应方程式:Pb+SO42--2e-=PbSO4
(2)写出镍镉电池放电时的总反应方程式:Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2
(3)使用铅蓄电池电解精炼铜,如果电解过程中转移了0.2mol电子,请计算:
①铅蓄电池内消耗硫酸的物质的量是0.2mol;
②生产精铜6.4克.
分析 (1)依据铅蓄电池的总反应方程式中元素化合价变化判断,负极失电子发生氧化反应;正极得到电子发生还原反应,负极 Pb+SO42-=PbSO4+2e-;正极 PbO2+4H++SO42-+2e-=PbSO4+2H2O;
(2)依据放电时的正极和负极反应书写放电时的总反应方程式;
(3)①根据铅蓄电池总反应式为 Pb+PbO2+2H2SO4 $?_{充电}^{放电}$2H2O+2PbSO4得出,消耗2moL硫酸转移2mol电子计算;
②根据精炼铜阴极反应为Cu2++2e-=Cu计算.
解答 解:(1)铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO4 $?_{充电}^{放电}$2H2O+2PbSO4;铅失电子生成硫酸铅,负极电极反应为:Pb+SO42--2e-=PbSO4,故答案为:Pb+SO42--2e-=PbSO4;
(2)镍镉碱性充电电池在放电时,正极反应为:2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-,负极反应为:Cd+2OH--2e-=Cd(OH)2,合并得到放电时的总反应方程式为:Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2;
故答案为:Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2;
(3)①由铅蓄电池总反应式为 Pb+PbO2+2H2SO4 $?_{充电}^{放电}$2H2O+2PbSO4得出,消耗2moL硫酸转移2mol电子,则电解过程中转移了0.2mol电子,铅蓄电池内消耗硫酸的物质的量是0.2mol,故答案为:0.2;
②因为精炼铜阴极反应为Cu2++2e-=Cu,所以电解过程中转移了0.2mol电子,则生产精铜6.4g,故答案为:6.4.
点评 本题考查了原电池的原理应用和电解原理应用,电极反应及其相关计算,电池反应是解题关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | Na2CO3溶液和稀盐酸 | B. | NaHCO3溶液和稀盐酸 | ||
| C. | AlCl3溶液和NH3•H20溶液 | D. | 澄清石灰水和NaHCO3溶液 |
| 物质 | N2 | Cl2 | Br2 | I2 | O2 |
| 键能 (kJ•mol-1) | 945 | 243 | 193 | 151 | 498 |
| 键长(nm) | 0.110 | 0.199 | 0.228 | 0.266 | 0.121 |
| A. | N2>Cl2>Br2>O2>I2 | B. | O2>N2>I2>Br2>Cl2 | ||
| C. | I2>Br2>Cl2>O2>N2 | D. | N2>O2>Cl2>Br2>I2 |
| A. | 金属钠加入水中:Na+H2O=Na++OH-+H2↑ | |
| B. | 碳酸氢钙溶液跟氢氧化钠溶液混合:HCO3-+OH-=CO32-+H2O | |
| C. | 氢氧化钡溶液滴入硫酸氢钠溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| D. | 亚硫酸钠和足量的稀硝酸混合:SO32-+2H+=SO2↑+H2O |
| A. | 过滤时,液面超过滤纸的边缘 | |
| B. | 加热试管内物质时,试管底部与酒精灯灯芯接触 | |
| C. | 过滤时,漏斗下端紧贴烧杯内壁 | |
| D. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 |
| A. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| B. | 实验室制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 | |
| C. | 单质硅是生产光纤制品的基本原料 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | V1≤V2 |
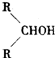 最难
最难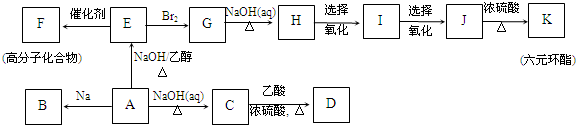
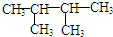 ,K为
,K为 ;
;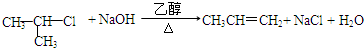 ;G→H
;G→H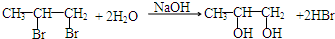 ;
;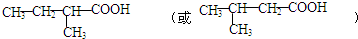 .
.