题目内容
9.已知NaHCO3溶液呈碱性,在NaHCO3溶液中,下列说法正确的是( )| A. | HCO3-的水解程度大于电离程度 | B. | HCO3-的水解程度小于电离程度 | ||
| C. | HCO3-的水解程度等于电离程度 | D. | 不能确定 |
分析 在NaHCO3溶液中,HCO3-既能水解又能电离,而HCO3-的电离显酸性,水解显碱性,根据NaHCO3溶液呈碱性来分析.
解答 解:在NaHCO3溶液中,HCO3-既能水解又能电离:HCO3-+H2O?H2CO3+OH-,HCO3-?CO32-+H+,而HCO3-的水解显碱性,电离显酸性,根据NaHCO3溶液呈碱性可知,HCO3-的水解程度大于电离程度,故A正确.
点评 本题考查了酸式弱酸盐的水解和电离,应注意的是强碱的酸式弱酸盐溶液的酸碱性取决于酸式弱酸根的水解和电离程度的相对大小.

练习册系列答案
相关题目
20.用O2将HCl转化为Cl2,反应方程式为:4HCl(g)+O2(g)?2H2O(g)+2Cl2(g)+Q(Q>0)
一定条件下测得反应过程中n(Cl2)的实验数据如下.下列说法正确的是( )
一定条件下测得反应过程中n(Cl2)的实验数据如下.下列说法正确的是( )
| t/min | 0 | 2 | 4 | 6 |
| n(Cl2)/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
| A. | 0~2 min的反应速率小于4~6 min的反应速率 | |
| B. | 2~6 min用Cl2表示的反应速率为0.9 mol/(L•min) | |
| C. | 增大压强可以提高HCl转化率 | |
| D. | 平衡常数K(200℃)<K(400℃) |
17.某有机物X的结构简式如图所示,则下列有关说法中正确的是( )
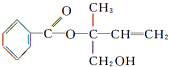

| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | 若单键可以旋转,有机物X中一定在同一平面上的碳原子数为8 | |
| D. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
4.下列说法正确的是( )
| A. | 蛋白质的水解可用于分离和提纯蛋白质 | |
| B. | 丙烯酸甲酯可通过缩聚反应生成高分子化合物 | |
| C. | 有机物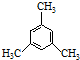 的核磁共振氢谱有两个峰,且峰面积之比为3:1 的核磁共振氢谱有两个峰,且峰面积之比为3:1 | |
| D. | 用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度 |
14.下列表示物质变化的式子错误的是( )
| A. | 氯气通入水中 Cl2+H2O?H++Cl-+HClO | |
| B. | 甲烷的完全燃烧CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$ CO2(g)+2H2O(l)△H<0 | |
| C. | 冰醋酸加入水中CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 铁与水蒸气反应 2Fe+3H2O$\frac{\underline{\;高温\;}}{\;}$ Fe2O3+3H2 |
18.X、Y、Z、R、W是原子序数依次增大的短周期元素,X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为19,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨.下列说法中正确的是( )
| A. | 最高价氧化物对应水化物酸性:X>R | |
| B. | 离子半径:Z>W | |
| C. | pH=10的Na2R溶液.由水电离出的c(H+)=10-10mol•L-1 | |
| D. | 气态氢化物稳定性:W>R |
12.如图所示的四个图象,能正确反映对应变化关系的是( )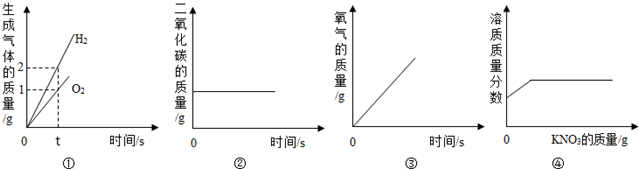

| A. | ①水的电解 | |
| B. | ②木炭在密闭的容器内燃烧 | |
| C. | ③加热一定量的高锰酸钾制氧气 | |
| D. | ④20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 |
 .
.