题目内容
下列说法正确的是( )
①标准状况下,22.4L己烯含有的分子数为NA
②标准状况下,22.4L氧气和氮气的混合物含有的分子数约为NA
③7.1g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.2NA
④1mol氨气中含有的共价键数约为4NA
⑤500mL1mol/L的硫酸铝溶液中含有的硫酸根离子数约为1.5NA.
①标准状况下,22.4L己烯含有的分子数为NA
②标准状况下,22.4L氧气和氮气的混合物含有的分子数约为NA
③7.1g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.2NA
④1mol氨气中含有的共价键数约为4NA
⑤500mL1mol/L的硫酸铝溶液中含有的硫酸根离子数约为1.5NA.
| A、①④ | B、②⑤ | C、③④ | D、②④ |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:①气体摩尔体积适用对象为气体;
②标况下,1mol任何气体体积均为22.4L;
③氯气和氢氧化钠反应是氯气自身氧化还原反应,1molCl2反应电子转移1mol;
④1个氨气分子含有3个N-H;
⑤依据硫酸铝化学式的构成离子和浓度体积与物质的量的换算关系计算判断.
②标况下,1mol任何气体体积均为22.4L;
③氯气和氢氧化钠反应是氯气自身氧化还原反应,1molCl2反应电子转移1mol;
④1个氨气分子含有3个N-H;
⑤依据硫酸铝化学式的构成离子和浓度体积与物质的量的换算关系计算判断.
解答:
解:①标况下,己烯属于液体,不能适用气体摩尔体积,故①错误;
②标准状况下,22.4L气体的物质的量=
=1mol,所以氧气和氮气的混合物含有的分子数约为NA,故②正确;
③7.1g氯气的物质的量为
=0.1mol,与足量的氢氧化钠溶液反应转移的电子数约为0.1NA,故③错误;
④1个氨气分子含有3个N-H,1mol氨气中含有的共价键数约为3NA,故④错误;
⑤500mL1mol/L的硫酸铝溶液中含硫酸铝物质的量为0.5mol,化学式Al2(SO4)3;所以含硫酸根离子物质的量为1.5mol,离子数约为1.5NA,故⑤正确;
故选:B.
②标准状况下,22.4L气体的物质的量=
| 22.4L |
| 22.4L/mol |
③7.1g氯气的物质的量为
| 7.1g |
| 71g/mol |
④1个氨气分子含有3个N-H,1mol氨气中含有的共价键数约为3NA,故④错误;
⑤500mL1mol/L的硫酸铝溶液中含硫酸铝物质的量为0.5mol,化学式Al2(SO4)3;所以含硫酸根离子物质的量为1.5mol,离子数约为1.5NA,故⑤正确;
故选:B.
点评:本题考查了阿伏伽德罗常数的应用,明确气体摩尔体积的条件应用,氧化还原反应的电子转移数计算,氨气子结构是解题关键,题目难度不大.

练习册系列答案
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
下列结构示意图所代表的微粒中,最难发生化学反应的是( )
A、 |
B、 |
C、 |
D、 |
如图是常见四种有机物的比例模型示意图.下列说法正确的是( )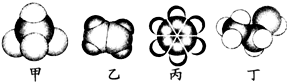

| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙可与溴水发生取代反应使溴水褪色 |
| C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的共价键 |
| D、丁与乙酸都能发生发生中和反应 |
室温下,下列各组离子在指定溶液中能大量共存的是( )
| A、甲基橙显黄色的溶液:AlO2-、HCO3-、Na+、K+ |
| B、c(H+)=1×10-1mol?L-1的溶液:IO3-、I-、K+、NH4+ |
| C、各离子物质的量浓度相等的溶液:K+、Na+、SO42-、NO3- |
| D、无色透明的溶液:NH4+、Na+、Cl-、CH3COO- |
下列叙述中正确的是( )
| A、含a mol AlCl3的溶液和含1.5a mol NaOH的溶液,无论正滴和反滴,生成的Al(OH)3的质量相等 |
| B、含a mol Na2CO3的溶液和含1.5a mol HCl的稀盐酸,无论正滴和反滴,生成的CO2相等 |
| C、等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D、二份质量相等组成不同的铝钠合金分别投入到足量盐酸中,若放出的H2越多,则铝的质量分数越小 |
化学在生产和日常生活中有着重要的应用.下列说法中不正确的是( )
| A、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
| C、用Al(OH)3制胃酸过多 |
| D、电解AlCl3饱和溶液,可制得金属铝 |
下列实验操作或对实验事实的叙述正确的是( )
| A、将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B、用碱式滴定管量取20.00mL0.1mol/LKMnO4溶液 |
| C、向沸腾的NaOH溶液中滴加FeCl3溶液,制备Fe(OH)3胶体 |
| D、配制FeSO4溶液时,需加入少量铁粉和稀硫酸 |
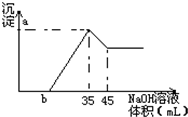 准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mLH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/LNaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.试求:
准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mLH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/LNaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.试求: