��Ŀ����
6���Ȼ�������SOCl2����һ��Һ̬������е�Ϊ77�棬��ũҩ����ҩ��ҵ����;�㷺��SOCl2��ˮ���ҷ�Ӧ��Һ���ϲ��������������д̼�����ζ�����������ʵ���Һϳ�ԭ����SO2+Cl2+SCl2�T2SOCl2������װ����ͼ��ʾ���ش��������⣺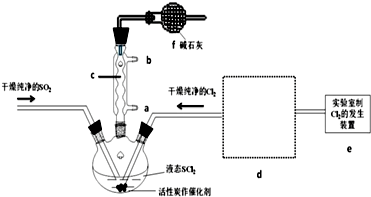
��1������c�����������������ܣ�װ��f�������������ݳ��ж���Cl2��SO2����ֹ�����е�ˮ�������뷴Ӧװ�ã���ֹSOCl2ˮ�⣮
��2��ʵ������Cl2�Ļ�ѧ����ʽΪMnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��3��SOCl2��ˮ��Ӧ�Ļ�ѧ����ʽΪSOCl2+H2O=SO2��+2HCl��������AlCl3��Һ���ܵõ���ˮAlCl3��ʹSOCl2��AlCl3•6H2O��ϼ��ȣ��ɵõ���ˮAlCl3���Խ���ԭ��AlCl3��Һ��ˮ�⣬AlCl3•6H2O��SOCl2��ϼ��ȣ�SOCl2��AlCl3•6H2O�еĽᾧˮ���ã�������ˮAlCl3��SO2��HCl���壬SOCl2��ˮ������SO2��HCl����AlCl3ˮ�⣮
��4�����������Ʊ�SO2�ķ��������ѡ���Ƕ���
| ���� | �� | �� | �� | �� |
| ����װ�� | 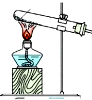 | 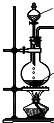 | 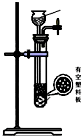 | 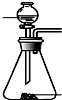 |
| ��ѡ�Լ� | NaHSO3���� | 18.4mol/LH2SO4 | 4mol/LHNO3+NaHSO3 | 70%NaHSO4+K2SO3 |
��6�����������������ƿ�л������뿪��ʵ�������������֪SCl2�ķе�Ϊ50�棩����Ӧ�����ĵ�Cl2�����Ϊ896mL����ת��Ϊ��״����SO2�����������õ�������SOCl2 4.76g����SOCl2�IJ���Ϊ50%��������λ��Ч���֣���
���� ��1����ͼ��֪��������ʯ�������巴Ӧ��
��2��ʵ��������MnO2��4HCl��Ũ���Ʊ�������
��3��SOCl2��ˮ��Ӧ�ķ���ʽΪ��SOCl2+H2O=SO2��+2HCl����AlCl3��Һ��ˮ�⣬AlCl3•6H2O��SOCl2��ϼ��ȣ�SOCl2��AlCl3•6H2O�еĽᾧˮ���ã�������ˮAlCl3��SO2��HCl���壬SOCl2��ˮ������SO2��HCl����ˮ����������ˮ�ⷢ����
��4�����й�����Һ�巴Ӧ��ȡ��������ȽϺ�������ȡ������Ҫ������������
��5��װ��e�в�����Cl2����d�����������ƿ��d�����������ҳ�ȥHCl��
��6����֪�Ȼ������е�Ϊ77�棬��֪SCl2�ķе�Ϊ50�棬���Բ��÷���ķ������ɽ�֮���룮��������Ϊ$\frac{0.896L}{22.4L/mol}$=0.04mol����SO2+Cl2+SCl2�T2SOCl2������0.08molSOCl2���Դ������
��� �⣺��1������c�����������ܣ�f����������һ���Ƿ�ֹ�ж�����������������ݳ���ʵ����Ա�����彡�������в��һ���Ƿ�ֹ�����е�ˮ����������ƿ��ʹ�Ȼ�����ˮ�⣬
�ʴ�Ϊ�����������ܣ������ݳ��ж���Cl2��SO2����ֹ�����е�ˮ�������뷴Ӧװ�ã���ֹSOCl2ˮ�⣻
��2��ʵ���������Ʊ��ķ���ʽΪMnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O���ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��3��SOCl2��ˮ��Ӧ�ķ���ʽΪ��SOCl2+H2O=SO2��+2HCl����AlCl3��Һ��ˮ�⣬AlCl3•6H2O��SOCl2��ϼ��ȣ�SOCl2��AlCl3•6H2O�еĽᾧˮ���ã�������ˮAlCl3��SO2��HCl���壬SOCl2��ˮ������SO2��HCl����ˮ����������ˮ�ⷢ����
�ʴ�Ϊ��SOCl2+H2O=SO2��+2HCl����AlCl3��Һ��ˮ�⣬AlCl3•6H2O��SOCl2��ϼ��ȣ�SOCl2��AlCl3•6H2O�еĽᾧˮ���ã�������ˮAlCl3��SO2��HCl���壬SOCl2��ˮ������SO2��HCl����AlCl3ˮ�⣻
��4����Ϊ���м�������������ȷʵ���������������ͬʱҲ������ˮ������������б�Թ���Ȼ�Dz��У�����18.4mol/L������̫Ũ������ˮ�ֹ���������Ȼ�Էַ�����ʽ���ڣ�����ͭ��Ӧ��ȡ������������������Ũ���ỹ��ϡ���ᶼ���к�ǿ�������Կ������Ľ����������е���4�۵�������Ϊ��6�۵���������Ӷ����õ����������з�Ӧ��������������������ˮ������ȡ��������ȽϺ������ʴ�Ϊ������
��5��װ��e�в�����Cl2����d�����������ƿ��d�����������ҳ�ȥHCl����d�����߿��ڻ�������ʵ��װ��ͼ��������Լ�Ϊ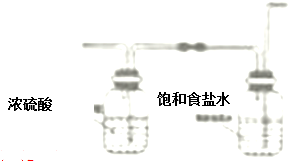 ��
��
�ʴ�Ϊ�� ��
��
��6����֪�Ȼ������е�Ϊ77�棬��֪SCl2�ķе�Ϊ50�棬���Բ��÷���ķ������ɽ�֮���룻��������Ϊ$\frac{0.896L}{22.4L/mol}$=0.04mol����SO2+Cl2+SCl2�T2SOCl2������0.08molSOCl2����SOCl2�IJ���Ϊ$\frac{4.76g}{0.08mol��119g/mol}$��100%=50%��
�ʴ�Ϊ������50%��
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ�߿��������ͣ������Ʊ�ʵ�鼰�����ķ�ӦΪ���Ĺؼ���������ѧ���ķ���������ʵ�������Ŀ��飬ע�ⳣ��������Ʊ�ԭ����Ӧ�ã���Ŀ�ѶȲ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | 2.7g���������������ʱʧȥ�ĵ�����ĿΪ0.1NA ����ʾ��M��Al��=27g/mol�� | |
| B�� | 17g���������ĵ�����ĿΪ10NA ����ʾ��M��NH3��=17g/mol�� | |
| C�� | 2g��������ԭ����ĿΪNA ����ʾ��M��H2��=2g/mol�� | |
| D�� | ���³�ѹ�£�11.2L����������ԭ����ĿΪNA |
| A�� | ��������������������������� | |
| B�� | �ᴿ���е���Ȼ�泥����������� | |
| C�� | ��ȥ̼�����е�����̼�����ƣ����ü��ȷ� | |
| D�� | ��ȥCO2�е�SO2��ͨ��ʢ����ˮ��ϴ��ƿ |
ʵ��������������������̨�����շ���������Ͳ���ձ�����Ƥ�ܡ��������ܡ���Һ©����
��֪�±��и������ڳ���ʱ���ܽ�ȣ�g/100gˮ��
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
��2��Ϊ��֤�Ƶõ�Na2CO3��Һ��������Ӧѡ�õ�ҩƷ�����ţ������⣬����Ҫ�ܢݣ�
��3����Ҫ����ʵ�鲽�裬ֱ���Ƶô�Na2CO3��Һ��������װ��ʡ�ԣ�����ȡһ������NaOH��Һ���ֳ����ȷݢ���ȡCO2��������һ��NaOH��Һ��ͨ�������CO2����۽�����Һ��Ͼ��ȣ�
��4�����ݸ������ܽ�ȱ��������NaOH��Һ�����ʵ������������ڶ���ʱ�������ƹ����л��о���������д�����㲽��ͱ�Ҫ������˵����
��ȷ�IJ���˳���ǣ�������
| A�� | �ڢۢ٢ݢ� | B�� | �٢ڢۢݢ� | C�� | �ۢ٢ڢܢ� | D�� | �٢ݢڢۢ� |
| A�� | ���������Һ��ͨ������Ķ�����̼Ca2++2ClO-+H2O+CO2=CaCO3��+2HClO | |
| B�� | ����������Һ�м������������ҺFe2++2H2O2+4H+=Fe3++4H2O | |
| C�� | �ð�ˮ����������������OH-+SO2=HSO3- | |
| D�� | ��������Һ���������ˮ3NH3•H2O+Fe3+=Fe��OH��3��+3NH4+ |
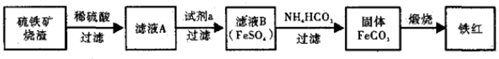
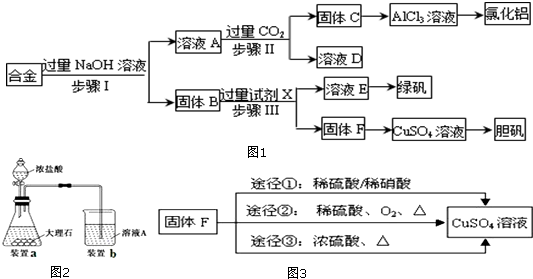
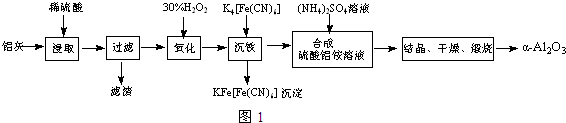
 ��2����30%��H2O2��Һ��Ŀ��������Fe2+ΪFe3+���������ڳ��������г�ȥ��
��2����30%��H2O2��Һ��Ŀ��������Fe2+ΪFe3+���������ڳ��������г�ȥ��