题目内容
在实验室里使稀盐酸与锌起反应,在标准状况时生成5.6L氢气,计算:
(1)需要多少摩的锌?
(2)需要2mol/L 的盐酸多少mL?
(1)需要多少摩的锌?
(2)需要2mol/L 的盐酸多少mL?
考点:化学方程式的有关计算
专题:计算题
分析:根据n=
计算5.6L氢气的物质的量,再根据方程式Zn+2HCl=ZnCl2+H2↑计算Zn、HCl的物质的量,根据V=
计算需要盐酸的体积.
| V |
| Vm |
| n |
| c |
解答:
解:5.6L氢气的物质的量=
=0.25mol,则:
Zn+2HCl=ZnCl2+H2↑
0.25mol 0.5mol 0.25mol
故需要2mol/L 盐酸的体积=
=0.25L=250mL,
答:(1)需要锌的物质的量0.25mol;
(2)需要2mol/L 盐酸250mL.
| 5.6L |
| 22.4L/mol |
Zn+2HCl=ZnCl2+H2↑
0.25mol 0.5mol 0.25mol
故需要2mol/L 盐酸的体积=
| 0.5mol |
| 2mol/L |
答:(1)需要锌的物质的量0.25mol;
(2)需要2mol/L 盐酸250mL.
点评:本题考查根据方程式进行的计算,比较基础,注意基础知识的理解掌握.

练习册系列答案
相关题目
下列各物质之间的反应属于置换反应的是( )
| A、CO还原氧化铜 |
| B、钠与稀盐酸反应 |
| C、铁与稀硝酸反应 |
| D、碳与浓硫酸反应 |
下列叙述正确的是( )
| A、金属与盐溶液反应都是置换反应 |
| B、阴离子都只有还原性 |
| C、与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
| D、在潮湿的环境下,黄铜(锌铜合金)比纯铜更耐腐蚀 |
能正确表示四种基本类型反应与氧化反应关系的示意图是( )
A、 |
B、 |
C、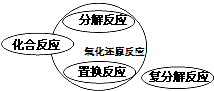 |
D、 |
 分类方法在化学学科的发展中起了非常重要的作用.图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子.对此反应的分类不正确的是( )
分类方法在化学学科的发展中起了非常重要的作用.图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子.对此反应的分类不正确的是( )| A、化合反应 | B、氧化还原反应 |
| C、可逆反应 | D、置换反应 |
等质量的下列物质完全燃烧时,消耗氧气的量最多的是( )
| A、C2H4 |
| B、C6H6 |
| C、C2H5OH |
| D、CH3COOH |
下列物质充分反应产生的气体体积(标准状况)最大的是( )
| A、100mL 2mol/L的稀硝酸与足量铜充分反应 |
| B、100mL 1mol/L盐酸与足量锌充分反应 |
| C、20mL 10mol/L浓盐酸与足量二氧化锰加热充分反应 |
| D、0.2molCu与足量18.4mol/L浓硫酸加热充分反应 |
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
| B、标准状况下,11.2L水所含分子数为0.5NA |
| C、同温同体积时,两种气体的压强比等于物质的量之比 |
| D、46gNO2和N2O4的混合物含有的分子数为NA |